Диагноз РС — клинико-визуализационный, требует подтверждения диссеминации в пространстве (признаков многоочагового поражения головного мозга) и во времени (несколько обострений по данным клинической или иной оценки или очаги различной давности при МРТ с контрастным усилением).
При несоблюдении одного из условий, для своевременной постановки диагноза используются данные о наличии олигоклональных антител в ликворе.
Магнитно-резонансная томография
МРТ — метод выбора для подтверждения клинического диагноза РС. Выявление на МРТ головного и спинного мозга очагов, гиперинтенсивных в Т2-режиме, накапливающих контраст, используется как суррогатный маркер обострения РС. МРТ имеет высокую чувствительность и специфичность — 87 и 73 %, соответственно и выявляет значительно больше очагов демиелинизации при РС, чем компьютерная томография (КТ). МРТ может выявить повреждения, расположенные в областях, изменения которых редко выявляются на КТ: ствол головного мозга, мозжечок и спинной мозг. Большинство очагов, выявленных на МРТ, подтверждается данными патологоанатомических исследований.
Характеристики очагов
Очаги на МРТ, характерные для РС, обычно выявляются в перивентрикулярных областях, мозолистом теле, семиовальном центре и, реже, в структурах подкоркового белого вещества и подкорковых ядрах. Очаги РС (бляшки) обычно овальной формы. Очаги, как правило, распространяются от мозолистого тела под прямым углом; при оценке изображений на сагиттальных срезах, такой характер изменений называется пальцы Доусона. Очаги РС имеют повышенную интенсивность на протонной плотности и T2-взвешенных изображениях. Многие очаги, особенно которые отмечаются длительно, гипоинтенсивные на T1-взвешенных изображениях (так называемые, «чёрные дыры»); другие становятся совсем неразличимыми.
При использовании стандартных T2-взвешенных последовательностей МРТ, возможна недооценка размера бляшек РС, их общего количества, в особенности в корковых областях. Дополнительные последовательности МРТ, такие как диффузионно-взвешенные изображения и МР-спектроскопия, часто выявляют вовлечение участков белого вещества пациентов РС сигнал от которых, при использовании других последовательностей, нормальный. Однако, ввиду высокой частоты встречаемости неспецифических поражений головного мозга, высок риск ложноположительных результатов. Более того, изменение диагностических критериев McDonald в 2017 году, вероятно, сделает эту проблему более значимой.
МРТ спинного мозга
Очаги при проведении МРТ спинного мозга у больных РС выявляются также часто, как и очаги головного мозга, при этом, первые чаще бывают бессимптомными. У здоровых лиц, напротив, частота выявления патологических сигналов на МРТ спинного мозга составляет всего 2%, поскольку, не связанные с РС гиперинтенсивные изменения сигнала на МРТ головного мозга, характерные для пожилых людей, не отмечаются в спинном мозге.
МР-характеристики типичных очагов в спинном и головном мозге сходны.
Перифокальный отёк ткани спинного мозга незначителен или не отмечается.
- Очаги имеют чёткий гиперинтенсивный характер на T2-взвешенных последовательностях и отмечаются в двух срезах (аксиальном или сагиттальном).
- Размер очагов не менее 3 мм, но, как правило, меньше двух сегментов спинного мозга. Занимают только часть поперечника спинного мозга и, обычно, располагаются в дорсолатеральной части спинного мозга.
- Ограниченные (чётко отличаются от окружающих тканях на T2-взвешенных последовательностях)
Дополнительное проведение МРТ спинного мозга может увеличить вероятность выявления диссеминации очагов в пространстве и повысить диагностическую чувствительность, по сравнению с проведением только МРТ головного мозга. Возможная диагностическая ценность МРТ спинного мозга при РС показана в исследовании с участием 104 пациентов на ранней стадии РС, имеющих низкую степень инвалидизации (Bot JC, Barkhof F, 2004). Постановка диагноза РС проводилась в соответствии с критериями Poser с соавт. (1982). Патологические очаги на МРТ спинного мозга были выявлены у 83%, очаги были фокальными; фокальные очаги чаще были множественными (медиана количества 3), небольшого размера (медиана размера 0,8 позвоночного сегмента) и локализованными преимущественно в шейном отделе позвоночника (56%). Диффузное поражение было выявлено у 13%, обычно сочеталось с выявлением очагов. В этой группе пациентов, оценка спинного мозга, в дополнение к МРТ головного мозга, в сравнении с проведением только МРТ головного мозга, повышало диагностическую чувствительность оригинальных критериев McDonald (2001) с 66 до 85%.
Большая протяжённость очагов спинного мозга, особенно, если она превышает три сегмента спинного мозга; если поражение вовлекает преимущественно центральные отделы спинного мозга на аксиальных срезах МРТ, характерны для оптиконевромиелита или сходных заболеваний.
Сравнительные характеристики острых и хронических очагов
Острые очаги РС на МРТ, как правило, более крупные, чем хронические и имеют несколько размытые границы. По мере разрешения, они уменьшаются в размере, края становятся более ровными. Эти изменения отражают прежде всего уменьшение отёка и воспаления, возникающих при формировании активной бляшки; с достижением ремиссии; остаются только резидуальная область демиелинизации, глиоза и увеличенные межклеточные пространства. МР-картина первично-прогрессирующего рассеянного склероза представлена меньшей распространённостью изменений, большей встречаемостью небольших очагов, меньшим количеством новых очагов, накапливающих гадолиниевый контраст, для неё характерно менее активное появление очагов в единицу времени, чем при вторично-прогрессирующей форме РС (Ingle GT, Thompson AJ, 2002).
Гадолиний-ДТПА, парамагнитное контрастное вещество, которое может проникать только через повреждённый гематоэнцефалический барьер и помогает выявлять активные очаги повреждения. Гадолиний повышает интенсивность сигнала на T1-взвешенных изображениях. Нет однозначного мнения о том, что воспаление является провоцирующим фактором, вызывающим демиелинизацию и аксональную дегенерацию, однако интенсивность «окраски» гадолиниевым контрастом уменьшается или исчезает после лечения глюкокортикоидами, терапия восстанавливает целостность гематоэнцефалического барьера.
Очаги накопления гадолиниевого контраста на T1-взвешенных последовательностях МРТ часто соответствуют областям повышенного сигнала на T2-взвешенных изображениях и низкой интенсивности сигнала на T1-взвешенных изображениях без контрастного усиления, возможно, ввиду отёка. Важность очагов накопления гадолиниевого контраста при РС подтверждается следующими фактами:
- Накопление гадолиния в бляшках указывает на развитие новых и активизацию старых очагов РС, что подтверждается данными гистологических исследований.
- Большинство очагов, накапливающих контраст, не имеют клинических проявлений, однако, такие изменения указывают на сохраняющуюся активность заболевания, способствующую прогрессированию повреждения мозга.
- Гадолиниевое усиление — транзиторный феномен, обычно исчезающий через несколько недель, но в редких случаях, он может продолжать отмечаться в острых бляшках в течение восьми недель. В одном исследовании было установлено, что средняя продолжительность времени, когда отмечается усиление составляет три недели, медиана продолжительности — две недели. Длительное сохранение очагов, накапливающих контраст, требует пересмотреть диагноз РС (Cotton F, Weiner HL, 2003).
- В долговременных исследованиях показано сочетание активных очагов на сериях МР-изображений с высоким риском длительной активности заболевания (Molyneux PD, Filippi M, 1998; Simon JH. 1999).
Особенности гадолиниевого усиления дают ценную информацию о патологических механизмах развития очагов. Концентрические очаги накопления контраста без контрастирования центральных частей очагов на месте прежних очагов или в областях усиленного фокального воспаления. Они более крупных размеров и сохраняются более длительно, чем очаги с однородным усилением. Однако, кольцевидные усиления редко сочетаются с развитием гипоинтенсивных поражений на МРТ в T1 режиме.
Поэтому, кольцевидные очаги связываются с повышением активности заболевания и распространённым поражением ткани и могут быть признаком воспалительных изменений, более характерных для агрессивных форм заболевания. Кольцевидное усиление может развиваться в виде неполных (разомкнутых) колец, что более характерно для РС, чем для инфекционных и опухолевых заболеваний.
Чёрные дыры
Большинство очагов РС изоинтенсивны по отношению к белому веществу на T1-взвешенных МР-изображениях, однако, некоторые из них, гипоинтенсивны или выглядят как «чёрные дыры», что особенно характерно для супратенториальных очагов. Эти гипоинтенсивные очаги не имеют определённых временных характеристик, приблизительно половина из них приобретают характеристики нормальной мозговой ткани через несколько месяцев. Исчезновение чёрных дыр наиболее вероятно связано с ремиелинизацией и регрессом отёка (Bitsch A, Kuhlmann T, 2001).
Несмотря на скудность доказательных данных, персистирующие чёрные дыры рассматриваются как признаки тяжёлой демиелинизации и гибели аксонов. На патогистологическом уровне, как было показано в исследовании, сопоставливавшем данные МРТ и патологоанатомических исследований, причиной накопления персистирующих чёрных дыр, является прежде всего аксональное повреждение. Такие очаговые повреждения аксонов, вероятно, способствуют Валлеровской дегенерации нейронов. В противоположность этим данным, в другом исследовании чёрные дыры рассматриваются как признаки ремиелинизации (Barkhof F, Bruck W, 2003).
Усовершенствованные методы МРТ
На основании данных стандартных (конвенционных) последовательностей трудно отличить отёк при развитии острых бляшек от глиоза и демиелинизации на месте хронических. Кроме того, стандартные последовательности МРТ не могут различить другие проявления патологического процесса при РС, такие как демиелинизацию, ремиелинизацию, гибель аксонов и глиоз.
Фосфорная магнитно-резонансная спектроскопия (МРС) может оценить показатели метаболизма фосфолипидов, протонная МРС предоставляет информацию о других метаболитах, таких как N-ацетиласпартат (NAA, вещество, которое находится только в нейронах), креатинфосфат (Cr, источник энергии), соединения, содержащие холин (компоненты мембраны), и молочная кислота (МК). Хроническое течение РС сопровождается уменьшением количества NAA, по сравнению с количеством холина и Cr в головном мозге. Наиболее часто, это оценивается при помощи отношения NAA/Cr. Уменьшенное отношение означает гибель нейронов или аксонов, что соответствует данным патологоанатомических исследований, и протекает одновременно с развитием функциональных нарушений при РС. Более того, концентрация NAA во всём головном мозге может быть чувствительным суррогатным маркером нейрональной гибели при РС (Rigotti DJ, Inglese M, 2007,2012).
Диффузионно-взвешенные и диффузионно-тензорные последовательности МРТ, как и МРС, могут обеспечить информацией о распространённости гибели аксонов и диффузных изменений нормального белого вещества, а также, о динамике изменений серого вещества, которое на стандартных последовательностях выглядит нормально. Количественные методики МРТ, такие как отношение переноса намагниченности, всё чаще используются для оценки содержания миелина и количества аксонов.
Диффузионно-тензорные последовательности помогают проводить оценку фракционной анизотропии, что отражает соотношение объёма однонаправленного движения молекул воды к объёму разнонаправленного движения. Эта методика пригодна для оценки целостности проводящих путей белого вещества, у которого, в норме высокая степень анизотропии по причине линейного расположения структур с преимущественным движением воды вдоль миелинизированных волокон. Повреждение аксонов или миелиновых оболочек повышает диффузию воды через структуры проводящих путей и повышает фракционную анизотропию.
Белое вещество с обычными характеристиками, которое непосредственно прилежит к бляшкам на T2 изображениях, может давать аномальный сигнал со сниженной анизотропией. Например, в исследовании, в котором проводилась оценка 36 бляшек белого вещества головного мозга у 20 пациентов с РС при оценке при помощи фракционной анизотропии было установлено, что средний размер бляшек, уменьшившийся на 40%, был значительно больше (145%) по сравнению с размером при оценке при помощи обычных T2-последовательностей на МРТ.
Несмотря на то, что при РС поражается преимущественно белое вещество, вовлечение коркового серого вещества встречается нередко. Стандартные (конвенционные) T2-взвешенные последовательности МРТ могут недооценивать размер бляшек РС, их общее количество, в особенности в корковых областях. Визуализация поражений серого вещества может быть улучшена при использовании методик МРТ с индукцией магнитного поля 7 Тл, двух — и трёхмерных изображений в режиме FLAIR (режим с подавлением сигнала свободной воды), импульсной последовательности с применением двойной инверсии T1-взвешенных изображений, и диффузионно-тензорных изображений.
Радиологически изолированный синдром
Радиологически изолированный синдром (РИС) определяется как случайная находка на МРТ головного (чаще) или спинного мозга. Как правило, причиной направления на МРТ служит другое состояние, не связанное с подозрением на РС, — головная боль или травма.
Кроме аномалий белого вещества, у отдельных пациентов с РИС на МРТ в режиме импульсной последовательности с применением двойной инверсии выявлялись демиелинизирующие поражения коры головного мозга.
Характерные изменения белого вещества, у пациента, даже в отсутствии неврологических нарушений, могут быть основой для подозрения на РС. Для описания случайных находок на МРТ — изменений белого вещества, характерных для рассеянного склероза Okuda с соавт (2009) был предложен термин «радиологически изолированный синдром» (РИС).
Очаги у пациентов без характерных для рассеянного склероза симптомов в анамнезе, должны соответствовать критериям по внешнему виду и признакам диссеминации в пространстве: овоидные, с чёткой границей или однородные очаги, как с вовлечением мозжечка, так и без; гиперинтенсивные на T2 >3 мм и соответствующие как минимум трём из четырёх критериев Barkhof
(1) девять и более очагов, или один или более очагов накапливающих контраст,
(2) три или более перивентрикулярных очага,
(3) один или более юкстакортикальных очага, и
(4) один или более инфратенториальных очага; и характер изменений белого вещества ЦНС не соответствует сосудистому.
РИС — относительно редкое состояние. В исследовании с участием госпитализированных пациентов, распространённость составила 0,15% у лиц в возрасте 15–40 лет которым проводилось МР головного мозга по различным медицинским показаниям (Granberg T, Martola J, Aspelin P, 2013). В Шведском регионе с высокой распространённостью рассеянного склероза (заболеваемость в Швеции составляет 10,2/100,000 человек в год), частота вновь выявленных случаев РИС составила 0,8 на 100,000 человек в год (Forslin Y, Granberg T, Jumah A. A. ). В течение последующих 5 лет после выявления РИС, демиелинизирующий эпизод с неврологическими нарушениями развивался у 30% пациентов с РИС, и у двух третей — отмечено прогрессирование появлением визуализационных признаков новых поражений на МРТ (Labiano-Fontcuberta A, Benito-Leon J. 2016). В настоящее время РИС не является показанием для назначения болезнь-модифицирующего лечения.
В ретроспективном исследовании с участием 326 пациентов (218 женщин, средний возраст 34,5 лет в диапазоне 10–55 лет) проводилось МРТ до и после контрастного усиления по причине головной боли без диагноза рассеянного склероза или клинически изолированного синдрома, распространённость гиперинтенсивности белого вещества составила 51.5%.[63]Картина соответствующая «контактному <примыкание к коре>» критерию Barkhof выявлялась у 2,4% пациентов, а критерию Barkof 3 мм у 7,1%. Критериям McDonald соответствовали 24,4% (»контактные») и 34,5% — 3 мм. Соответствие «контактному» критерию предполагает перивентрикулярные очаги, прилежащие к желудочкам, а 3 мм критерии — перивентрикулярные очаги, отграниченные от желудочков 3 мм. Для сравнения, распространённость рассеянного склероза в общей популяции составляет 0,085% (Liu S, Kullnat J, Bourdette D, 2013).
Таблица
МРТ критерии диагностики рассеянного склероза MAGNIMIS (2016)
| Форма РС | Диссеминация в пространстве | Диссеминация во времени |
|---|---|---|
|
РРС |
Наличие очагов в двух из пяти типичных локализаций:
Не имеет значения симптомность очагов в стволе мозга, спинном мозге и зрительном нерве |
Один из следующих критериев:
|
|
ППРС |
Два из трех следующих критериев:
уровня IgG в ЦСЖ |
Прогрессирование заболевания в течение 1 года (определяемое ретроспективно и проспективно) |
Дополнительные методы исследования
Анализ спинномозговой жидкости (СМЖ) и определение СМЖ-специфических олигоклональных антител, оценка вызванных потенциалов, оптическая когерентная томография и тесты на аутоантитела могут использоваться для оценки случаев, когда предполагается рассеянный склероз, а данные клиники и МРТ недостаточны для подтверждения диагноза.
Анализ СМЖ и олигоклональные антитела
Ввиду развития аутоиммунных воспалительных изменений за гематоэнцефалическим барьером, у больных РС нет системных воспалительных изменений и наиболее точными лабораторными методами диагностики являются исследования ликвора.
При типичном течении заболевания и характерной МР-картине, для постановки диагноза РС не требуется проведение люмбальной пункции, однако, это может увеличить точность диагноза в следующих случаях:
- При поступлении пациента с клинически изолированным синдромом, указывающим на РС, при соответствии радиологическим критериям в отношении диссеминации в пространстве, но не во времени; критерии McDonald допускают выявление СМЖ-специфичных олигоклональных антител в качестве замены диссеминации во времени.
- Для пациентов с клинически изолированным синдромом, у которых данные МРТ не соответствуют критериям McDonald в отношении диссеминации в пространстве (т. е. на МРТ головного мозга не выявляется новых очагов или они выявляются в недостаточном количестве), поскольку оценка спинномозговой жидкости на олигоклональные антитела (IgG) может способствовать более точной оценке риска прогрессирования рассеянного склероза.
- При наборе симптомов, отличных от типичных проявлений клинически изолированного синдрома, включая прогрессирующее течение с момента начала (т. е. указаний на первично-прогрессирующий тип РС)
- При выявлении клинических, визуализационных и лабораторных характеристик, атипичных для РС.
- В группах пациентов с низкой частотой развития РС, например, у детей и пожилых.
Качественная оценка СМЖ на олигоклональные IgG антитела при использовании изоэлектрического фокусирования — сопровождающаяся одновременным проведением анализа сыворотки — наиболее важное исследование СМЖ, при определении диагноза РС.
Повторное проведение люмбальной пункции и оценки СМЖ предлагается, при обоснованном подозрении на РС на основании клинических данных, когда первичные анализы СМЖ противоречивы или отрицательны или показывают только одну полосу при изоэлектрическом фокусировании.
Олигоклональные антитела у пациентов с достоверным клиническим диагнозом РС выявляются с частотой до 95%. Олигоклональные антитела представляют собой ограниченные классы антител, которые отображаются в виде отдельных полос на агарозном геле. Суждение о положительном результате анализа основывается на выявлении характерных для олигоклональных антител полос, отличающихся от обычного состава сыворотки или на повышении индекса IgG. Уровень IgG может выражаться в процентах от общего белка (норма <11%), а также в процентах от количества альбумина (норма <27%), при использовании расчётного индекса IgG (нормальная величина <0,66 — <0.9, в зависимости от лаборатории), или при помощи формулы синтеза IgG в интратекальной жидкости.
Внешний вид СМЖ и давление у большинства пациентов с РС нормальные. Общее количество лейкоцитов соответствует норме приблизительно у трети пациентов, превышает 15/мкл у другой трети, и редко превышает 50/мкл (лабораторная находка, которая должна насторожить в отношении другой этиологии). Основным типом клеток являются лимфоциты, преимущественно — T-клетки. Уровень белка (или альбумина) в ликворе обычно нормальный. Альбумин не синтезируется в центральной нервной системе, таким образом, определение альбумина даёт более достоверные указания на нарушение целостности гематоэнцефалического барьера, чем общий белок (некоторые виды белковых молекул, например, иммуноглобулины) могут синтезироваться в центральной нервной системе.
До 8% образцов СМЖ, полученных от пациентов без РС, также содержат олигоклональные антитела, образование которых чаще всего связано с хроническими системными инфекциями центральной нервной системы, вирусными заболеваниями и невропатиями. В большинстве случаев, олигоклональные антитела также выявляются в анализе сыворотки. Выявление олигоклональных антител не означает установленного диагноза РС, ввиду большого количества ложно-положительных результатов и различий в методиках и их интерпретации в различных лабораториях. Повышение отношения иммуноглобулинов в СМЖ к другим белковым компонентам является распространённой находкой у пациентов с РС и указывает на их интратекальный синтез. Повышение концентрации иммуноглобулинов связано преимущественно с повышением концентрации IgG, однако, синтез иммуноглобулина M (IgM) и иммуноглобулина A (IgA) также повышается.
Вызванные потенциалы
Электрические сигналы, формирующиеся в центральной нервной системе под действием периферической стимуляции органов чувств. Вызванные потенциалы (ВП) используются для выявления субклинических нарушений функций нервной системы. Выявление субклинического повреждения в месте, удалённом от области, предполагаемой на основании клинических данных, указывает на многоочаговое поражение ЦНС. ВП могут установить анатомическую локализацию повреждения проводящих путей, которые плохо видны по данным визуализационных исследований (например, зрительных нервов, дорсальных колонн). Наиболее часто используются соматосенсорные, зрительные и акустические стволовые вызванные потенциалы.
У пациентов с клиническим диагнозом РС отклонения при исследовании зрительных вызванных потенциалов выявляются в 50–90% случаев. Наибольшее значение зрительных ВП при недостаточности объективных клинических проявлений симптомов выше уровня большого затылочного отверстия, например при хронической прогрессирующей миелопатии. Трактуя указания исследования зрительных ВП, как признаки демиелинизации зрительных путей, необходимо исключить нарушения зрения и патологию сетчатки.
Оптическая когерентная томография
При оптической когерентной томографии (ОКТ) используется инфракрасный свет, который выявляет микроструктуру биологических тканей на основе их способности к отражению, эта информация используется в построении изображений.
ОКТ обеспечивает возможность неинвазивной оценки сетчатки с высоким разрешением. Метод может использоваться для оценки толщины слоя волокон зрительного нерва сетчатки, которая снижена у 85% пациентов с невритом зрительного нерва. Демиелинизирующее поражение зрительного нерва и зрительного тракта приводят к ретроградной дегенерации потерявших оболочку аксонов в составе слоя волокон зрительного нерва сетчатки. Уменьшение толщины этого слоя начинает отмечаться на ОКТ приблизительно через 3 месяца после перенесённого неврита зрительного нерва. Роль ОКТ в установлении диагноза РС недостаточно изучена. Однако исследование может оценить состояние сетчатки у пациентов с указаниями на симптомы неврита зрительного нерва в анамнезе, что важно при нормальном результате нейровизуализации. Кроме того, отдельные данные указывают на меньшую толщину слоя волокон зрительного нерва и ганглиозного слоя при расстройствах спектра оптикомиелита по сравнению с рассеянным склерозом, что может быть полезным в дифференциальном диагнозе этих расстройств.
Исследование антител
В ткани головного мозга за гематоэнцефалическим барьером возможен синтез иммуноглобулинов. При этом, повышается их концентрация как в абсолютных величинах, так в отношении к концентрации в плазме крови (коэффициенты QIgG, QIgA, QIgM, практическое значение имеет только определение QIgG). В норме QIgG не превышает 6 × 10–3. Для оценки локального синтеза IgG используют номограммы зависимости Q(альб) против QIgG, основанные на математической модели проницаемости гематоэнцефалического барьера.
В норме QIgG не превышает 6 × 10-3. Для оценки локального синтеза IgG используют номограммы зависимости Q(альб) против QIgG, основанные на математической модели проницаемости гематоэнцефалического барьера (Gama P. D. 2002).
Исследование на антитела (IgG) к аквапорину-4 (AQP4) и миелиновому олигодендроцитарному гликопротеину (MOG-IgG) показано пациентам атипичными для РС данными клинических, лабораторных и визуализационных исследований.
Антитела AQP4
Антитела к AQP4 являются специфическим биомаркером спектра оптикомиелит-ассоциированных расстройств (СОМАР), поэтому, пациентам с подозрением на СОМР показано исследование антител AQP4 IgG в крови.
Клинические признаки, указывающие на возможность СОМАР
- одновременное развитие двустороннего неврита зрительного нерва с вовлечением хиазмы, горизонтальной гемианопсии или развитием резидуальных зрительных нарушений
- полное, а не частичное поражение спинного мозга, особенно, сопровождающееся пароксизмальными тоническими спазмами; на МРТ позвоночника выявляется продольное поражение спинного мозга с интенсивным сигналом, распространяющееся на три более сегмента позвоночника.
- некупируемая икота или тошнота со рвотой вследствие поражения самого заднего поля (area postrema) — участок ромбовидной ямки, расположенный кзади и латерально от треугольника блуждающего нерва; в пределах поля частично проецируются ядра блуждающего нерва.
IgG антитела к миелиновому олигодендроцитарному гликопротеину
Антитела к миелиновому олигодендроцитарному гликопротеину (MOG-IgG) являются маркером MOG-ассоциированного энцефаломиелита, относительно редкого демиелинизирующего заболевания, характеризующегося различными проявлениями, включая рецидивирующий и двусторонний неврит зрительного нерва, поперечный миелит, стволовой энцефалит и острый диссеминированный энцефаломиелит (ОРЭМ). Показания к анализу на MOG-IgG проводятся в приложении.
Таблица
Вспомогательные методы исследования при рассеянном склерозе
| Метод исследования | Распространённость нарушений у больных РС (%) |
|---|---|
|
Зрительные вызванные потенциалы |
50–90 |
|
Акустические стволовые вызванные потенциалы |
20–55 |
|
Соматосенсорные вызванные потенциалы |
50 |
|
Олигоклональные антитела в спинномозговой жидкости |
85–95 |
|
Индекс IgG в спинномозговой жидкости |
75 |
|
МРТ головного мозга |
70–95 |
|
Общий анализ ликвора (плейоцитоз 6–20 (до 50) в мкл) |
30 |
- Giesser BS. Diagnosis of multiple sclerosis. Neurol Clin 2011; 29:381.
- Dobson R, Ramagopalan S, Davis A, Giovannoni G. Cerebrospinal fluid oligoclonal bands in multiple sclerosis and clinically isolated syndromes: a meta-analysis of prevalence, prognosis and effect of latitude. J Neurol Neurosurg Psychiatry 2013; 84:909.
Таблица
Критерии диагностики рассеянного склероза у пациентов во время приступа в начале заболевания McDonald (2017)
| Количество очагов с объективными клиническими симптомами | Дополнительные данные, необходимые для установления диагноза рассеянного склероза | |
|---|---|---|
|
≥2 обострений с клиническими симптомами |
≥2 |
Не требуется* |
|
1 (а также, явные клинические признаки перенесённого ранее обострения, в сочетании с очагом в соответствующей анатомической области¶) |
Не требуется* |
|
|
1 |
Диссеминация в пространстве, установленная на основании дополнительного клинического приступа, связанного с поражением другого участка ЦНС, или по данным МРТ |
|
|
1 обострение |
≥2 |
Диссеминация во времени, установленная на основании дополнительного приступа или при помощи МРТ ИЛИ выявлении СМЖ-специфических олигоклональных антител§ |
|
1 |
Диссеминация в пространстве, установленная на основании дополнительного клинического приступа, связанного с поражением другого участка ЦНС, или по данным МРТ И Диссеминация во времени, установленная на основании дополнительного приступа или при помощи МРТ◊ ИЛИ выявлении СМЖ-специфических олигоклональных антител§ |
¶ Наиболее достоверным является клинический диагноз, установленный на основании клинических данных о двух приступах. Достоверные анамнестические данные об одном обострении, перенесённом в прошлом, в отсутствии задокументированных объективных неврологических нарушений, могут включать, могут включать анамнестические указания на симптомы и их динамику, характерные для перенесённых ранее приступов воспалительной демиелинизации; однако, не менее одного обострения должно подтверждаться объективными данными.
§ Выявление СМЖ-специфических олигоклональных антител само по себе не подтверждает диссеминации во времени, однако, может быть заменой этому критерию.
* Не требуется проведение дополнительных исследований, чтобы показать диссеминацию в пространстве и времени. Однако, за исключением случаев, когда проведение МРТ невозможно, всем пациентам с предположительным диагнозом «рассеянный склероз» требуется проведение МРТ головного мозга. Кроме того, пациентам с недостаточным набором клинических данных и МРТ-признаков, подтверждающих диагноз «рассеянный склероз», дебютом, отличным от характерных проявлений клинически изолированного синдрома, требуется проведение МРТ спинного мозга или оценка СМЖ. При отрицательных результатах нейровизуализации или других методов исследования (например, СМЖ), до постановки диагноза «рассеянный склероз» необходимо рассмотреть альтернативные диагнозы.
Рассеянный склероз диагностируется, если случай соответствует критериям McDonald (2017 ) и не имеет лучшего объяснения другим диагнозам. Если диагноз рассеянного склероза предполагается на основании клинически изолированного синдрома, но случай не соответствует полному набору критериев McDonald (2017 ), выставляется диагноз «возможный рассеянный склероз». Если при оценке пациента устанавливается другой диагноз, лучше объясняющий симптомы пациента, диагноз рассеянный склероз не выставляется.
ЦНС: центральная нервная система; МРТ: магнитно-резонансная томография; СМЖ: спинномозговая жидкость.
Критерии McDonald для диссеминации в пространстве
Диссеминация в пространстве определяется как развитие очагов в различных анатомических областях центральной нервной системы, что указывает на многоочаговый процесс.
Соответствие критериям McDonald для диссеминации в пространстве устанавливается если состояние пациента с клинически изолированным синдромом или типичным обострением РС соответствует одному из следующих утверждений:
- На МРТ не менее 1 очага с гиперинтенсивностью в T2, характерных для рассеянного склероза, не менее чем в двух из четырёх областей типичного расположения очагов РС в центральной нервной системе:
- Перивентрикулярные области
- Кортикальные или юкстакортикальные области
- Инфратенториальные области
- Спинной мозг
- Развитие ещё одного обострения с клиническими признаками, характерными для рассеянного склероза, по данным клинического осмотра, указывающего на поражение другого отдела центральной нервной системы.
Критерии McDonald для диссеминации во времени
Диссеминация во времени требует наличия появления новых очагов в центральной нервной системе с течением времени.
Соответствие критериям McDonald для диссеминации во времени устанавливается если состояние пациента с клинически изолированным синдромом или типичным обострением РС соответствует одному из следующих утверждений:
- Развитие ещё одного обострения с клиническими признаками, характерными для рассеянного склероза, по данным клинического осмотра.
- МРТ головного мозга и/или спинного мозга выявляет одновременное наличие очагов, накапливающих и не накапливающих гадолиниевый контраст, или появление новых очагов, гиперинтенсивных в T2-режимах и/или при использовании гадолиниевого контраста на МРТ во время динамического наблюдения, вне зависимости от времени с момента исходного исследования.
- Выявление специфических олигоклональных антител в ликворе (как замена признака диссеминации во времени)
Обострение
Обострение определяется как монофазный клинический эпизод с развитием симптомов,
- описываемых пациентом и имеющих объективные проявления, характерные для рассеянного склероза,
- указывающих на очаговое или многоочаговое воспалительное демиелинизирующее поражение ЦНС с острым или подострым развитием,
- продолжительностью не менее 24 часов, с восстановлением или без восстановления нарушенных функций и
- в отсутствии лихорадки или признаков инфекционного заболевания.
Термины «атака», «обострение» или «экзацербация» и (если это первый эпизод) «клинически изолированный синдром», являются синонимами.
Объективные клинические проявления
Обострение РС должно подтверждаться объективными клиническими проявлениями: неврологическими нарушениями, данными визуализации (МРТ или оптическая когерентная томография) или нейрофизиологического исследования (зрительные вызванные потенциалы), соответствующие анатомической локализации очага, отвечающего за развитие симптомов текущего или установленного по данным анамнеза обострения.
Например, эпизод перенесённых болезненных монокулярных зрительных нарушений, соответствующих невриту зрительного нерва, должен подтверждаться выявлением побледнением диска зрительного нерва или относительным афферентным зрачковым дефектом (зрачок Маркуса-Гунна), гиперинтенсивностью зрительного нерва в T2-режиме, истончением слоя волокон зрительного нерва сетчатки на оптической когерентной томографии или увеличением латентности P100 при исследовании вызванных зрительных потенциалов.
Дифференциальный диагноз рассеянного склероза
- Острый диссеминированный энцефаломиелит
- Болезнь Бехчета
- CLIPPERS – хроническое лимфоцитарное воспаление с поражением моста, контрастным усилением периваскулярных пространств в мосту по данным магнитно-резонансной томографии, отвечающее на терапию глюкокортикостероидными препаратами
- Клинически изолированный синдром с признаками рассеянного склероза
- Миелин-ассоциированный гликопротеин IgG-ассоциированный энцефаломиелит
- Расстройства спектра оптикомиелита
- Паранеопластические энцефаломиелопатии
- Узелковый полиартериит
- Первичный ангиит центральной нервной системы
- Синдром Шёгрена
- Системная красная волчанка
- Инфекционные заболеваниями
- Вирус иммунодефицита человека
- Болезнь Лайма (нейроборрелиоз)
- Нейросифилис
- Прогрессирующая мультифокальная лейкоэнцефалопатия
- Тропический спастический парапарез/HTLV-1-ассоциированная миелопатия
- Генетические заболевания
- Церебральная аутосомная доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией (CADASIL)
- Гранулёматозные заболевания
- Лимфоматоидный гранулёматоз
- Саркоидоз
- Гранулёматоз с полиангиитом (болезнь Вегенера)
- Миелинопатии
- Адренолейкодистрофия
- Метахроматическая лейкодистрофия взрослых/лейкодистрофия Шольца-Гринфилда
Другие
- Аномалия Арнольда-Киари
- Компрессионное поражение спинного мозга
- Сосудистые мальформации
- Дефицит витамина B12
- Спиноцеребеллярные нарушения
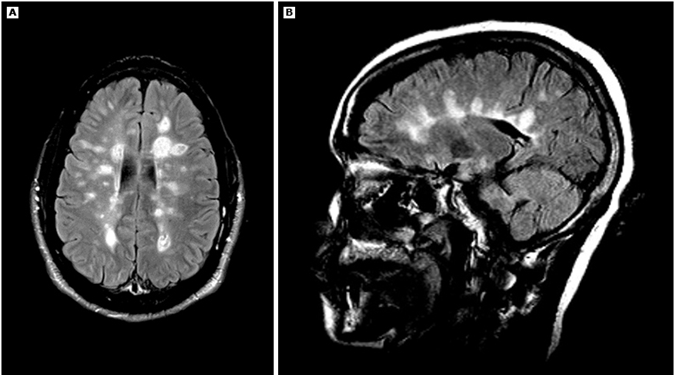
Рисунок
Аксиальные (A) и сагиттальные срезы (B) МРТ (FLAIR) головного мозга, на которых видны множественные овоидные перивентрикулярные очаги (пальцы Доусона) у пациента с рассеянным склерозом.
Наблюдение пациента в динамике
С целью оценки прогрессирования заболевания, каждые 3–6 месяцев повторяется полный неврологический осмотр, дополнительно проводится функциональная оценка двигательных и когнитивных функций пациента, эмоционально-волевой сферы при помощи специализированных шкал.
Повторные МРТ головного мозга с контрастным усилением целесообразно проводить каждые 6–12 месяцев и при клиническом ухудшении состояния. МРТ спинного мозга проводятся только по показаниям (преимущественное или изолированное поражение спинного мозга, указания на острое развитие симптомов, топически связанных со спинным мозгом). Кратность проведения исследований в динамике по данным консенсусных рекомендаций противоречива (Luzzio C. Chawla J. 2018).
Ежегодно или при ухудшениях, целесообразна консультация специалиста по двигательным расстройствам.
Стандартным указанием на прогрессирование РС служит повышение на один и более баллов оценки по шкале инвалидизации Курцке (EDSS, функциональная оценка прогрессирования заболевания), которое сохраняется при повторной оценке через 3 месяца.
Для оценки качеств жизни пригодны такие инструменты как Multiple Sclerosis Impact Scale <Шкала оценки дефекта при рассеянном склерозе> (MSIS-29).
Набор необходимых лабораторных анализов включает:
- общий анализ крови + СОЭ,
- общий анализ мочи,
- биохимический анализ крови (креатинин, общий и прямой билирубин, общий белок, глюкоза, общий холестерин, АЛТ, ACT).