НКР, вызванное болезнью Альцгеймера
Диагностические критерии DSM-5
A. Соответствие критериям большого или малого нейрокогнитивного расстройства.
B. Незаметное начало и постепенное прогрессирование нарушение в одном или нескольких доменах когнитивных функций (для постановки диагноза большого нейрокогнитивного расстройства необходимо наличие нарушений не менее чем в двух доменах).
C. Критерии, соответствующие вероятной или возможной болезни Альцгеймера, включают следующие:
Для большого нейрокогнитивного расстройства:
Вероятная болезнь Альцгеймера диагностируется, если верно одно из следующих утверждений; в противном случае устанавливается возможная болезнь Альцгеймера.
1. Признаки генетической мутации, приводящей к развитию болезнь Альцгеймера по данным семейного анамнеза или генетического тестирования.
2. Верны все три из нижеперечисленных утверждений:
a. Убедительные признаки нарушения памяти и способности к обучению не менее чем в одном из когнитивных доменов (на основании анамнеза или подробного нейропсихологического тестирования).
b. Неуклонное прогрессирование, постепенное усиление когнитивных нарушений без продолжительных периодов стабилизации (»плато»).
c. Нет признаков смешанной этиологии (отсутствие других нейродегенеративных или цереброваскулярных заболеваний или других неврологических, психических или системных заболеваний или состояний, способствующих развитию когнитивных нарушений).
Для малого нейрокогнитивного расстройства:
Вероятная болезнь Альцгеймера диагностируется при наличии признаков генетической мутации, вызывающей болезнь Альцгеймера, по данным семейного анамнеза.
Возможная болезнь Альцгеймера диагностируется в отсутствии признаков генетической мутации, вызывающей болезнь Альцгеймера, по данным семейного анамнеза или генетического тестирования если верны все три из нижеперечисленных утверждений:
1. Убедительные признаки нарушения памяти и способности к обучению.
2. Неуклонное прогрессирование, постепенное усиление когнитивных нарушений без продолжительных периодов стабилизации (»плато»).
3. Нет признаков смешанной этиологии (отсутствие других нейродегенеративных или цереброваскулярных заболеваний или других неврологических, психических или системных заболеваний или состояний, способствующих развитию когнитивных нарушений).
D. Нарушение не имеет лучшего объяснения цереброваскулярным заболеванием, другим нейродегенеративным заболеванием, действием наркотических препаратов, другим психическим, неврологическим или системным заболеванием.
НКР, вызванное лобно-височной дегенерацией
Лобно-височные деменции (ЛВД, болезнь Пика) — одна из наиболее распространённых причин раннего развития деменции — группа разнородных нейродегенеративных заболеваний с прогрессирующими поведенческими и личностными нарушениями, постепенной утратой эмпатии и способности к продуктивному контакту. В основе ЛВД лежит дегенерация лобных и передних отделов височных долей.
Медианный возраст развития ЛВД составляет 58 лет, диапазон возрастов — 20 — 80 лет. Мутации, которые можно рассматривать как причину заболевания, были выделены приблизительно у 40% от общего количества пациентов. Они включают C9ORF72 (наиболее частая форма ЛВД), тау-белок, ассоциированный с микротрубочками (MAPT) и програнулин (GRN).
Расторможенность — пациенты с расторможенностью не соблюдают социальную дистанцию, трогают и целуют незнакомых людей, проявляют вербальную и
физическую агрессию, публично обнажаются и мочатся, демонстрируют напыщенность, неподобающую ситуации. Пациенты с ЛВД могут демонстрировать примеры утилизационного поведения: бесцельно манипулировать предметами, находящимися в доступности, брать чужие вещи.
Апатия и утрата способности сопереживать — апатия проявляется потерей интереса и/или мотивации к повседневным делам и поддержанию социальных связей. Пациенты становятся более пассивными, меньше участвуют в обсуждениях. Часто апатия ошибочно воспринимается как депрессия (для последнего состояния, кроме снижения активности также характерно негативное представление о будущем, снижение самооценки). В исследовании Zucca M, Rubino E, 2018 указывается на кратно бо́льшую частоту суицидальных мыслей и попыток суицида у пациентов с поведенческим вариантом ЛВД в сравнении с контрольной группой.
Потерю пациентом способности сопереживать ухаживающие лица описывают как «холодность» и невосприимчивость к чужим эмоциям. К нарушениям способности к симпатии и эмпатии могут приводить дегенерация коры правой орбитофронтальной и передней височной области.
Гипероральность (навязчивое желание пробовать предметы «на зуб», постоянно что-то жевать) и изменение пищевых пристрастий, например, любовь к газировке, сладкой пище (что характерно и для больных с другими типами деменций), обжорство. Пища потребляется без достаточного пережёвывания. Может отмечаться повышенное, в сравнении с привычным, употребления алкоголя и табака. Пациенты могут пытаться употребить в пищу несъедобные продукты. Эти нарушения поведения соотносятся с дегенерацией правой лобно-орбитальной, островковой областей коры мозга, полосатого тела и гипоталамуса.
Компульсивное поведение — повторные стереотипные или навязчивые виды поведения, сходные с ритуалами, включая речевые стереотипии, повторяющиеся простые движения, и сложные стереотипии, такие как собирательство, склонность проверять или мыть окружающие предметы. Может появиться навязчивый счет (»арифмомания») — пациенты постоянно считают количество пройденных ступеней, сделанных шагов, зажженных окон. Эти изменения ошибочно связывают с обсессивно-компульсивным синдромом.
По мере развития заболевания постепенно снижается повседневная активность пациентов, возрастает нагрузка по уходу на окружающих, что усугубляется утратой эмоционального контакта с больными и их неадекватным поведением. В конечном итоге развиваются мутизм и полная социальная изоляция.
Пациенты часто не обращают достаточного внимания на изменения поведения и доставляют дискомфорт своим близким. Для того, чтобы выявить лёгкие поведенческие нарушения, может быть полезным задать ухаживающим лицам следующие вопросы:
- Было ли такое, что находясь в обществе, пациент делал или говорил вещи, возмутившие окружающих?
- Можно ли сказать, что пациент у пациента исчезло чувство отвращения?
- Выглядит ли пациент безразличным к чувствам других, менее «тёплым» и душевным, особенно, по отношению к внукам или животным?
- Поменялись ли пищевые предпочтения и застольные манеры пациента?
- Не стал ли пациент более озабоченным соблюдением графика, не чаще ли смотрит ли часы?
- Появились ли изменения в чувстве юмора пациента?
- Появились ли у пациента новые увлечения или интерес, граничащие с навязчивостями, особенно области религии и эзотерики?
Выделяются следующие варианты лобно-височной деменции:
Поведенческий вариант
Первичная прогрессирующая афазия (ППА)
- Вариант с преимущественным снижением речевой активности — преобладание трудностей с артикуляцией, плавным переключением между фонемами; речь становится замедленной с большим количеством аграмматизмов.
- Семантический вариант — основные трудности в выражении смысла одним словом, назывании предметов при сохранной речевой активности, понимании речи и повторении высказываний.
- Логопенический вариант — затруднения в воспроизведении отдельных слов, повторение с ошибками, при сохранной способности назвать предмет и отсутствии аграмматизмов
Двигательные нарушения, ассоциированные с лобно-височной дегенерацией
- синдром бокового амиотрофического склероза — деменции лобного типа,
- кортико-базальный синдром
- синдром прогрессирующего надъядерного паралича
У пациентов с поведенческим вариантом ЛВД, особенно в начале заболевания, крайне редко встречаются симптомы поражения черепных нервов, чувствительные, мозжечковые, пирамидные и экстрапирамидные симптомы. Наличие «лобных» знаков не специфично для этой группы больных и не имеет диагностической ценности. На более поздних стадиях набор стереотипных форм поведения становится более скудным, на первый план выходит когнитивный дефицит, отражающий дегенерацию медиальных отделов лобной коры. Появление паркинсонизма также характерно для более поздних стадий заболевания.
Специфических нейровизуализационных признаков ЛВД не описано. В начале — МРТ головного мозга не выявляет патологии, на поздних стадиях, примерно у половины пациентов встречаются локальные атрофические изменения лобных и височных долей.
Международные консенсусные критерии диагностики поведенческого варианта лобно-височной деменции
I. Нейродегенеративное заболевание
Прогрессирующее нарушение поведения и/или когнитивных функций по данным наблюдения или анамнеза (сообщаемого осведомленным близким).
II. Возможный диагноз ЛВД: не менее трех постоянных или часто повторяющихся (но не однократных или редко повторяющихся) поведенческих/когнитивных симптомов из следующих 6 групп (A–F):
A. Раннее развитие расторможенности — при наличии по крайней мере одного из следующих симптомов:
1) социально неуместное поведение,
2) утрата манер или внешних приличий,
3) импульсивные, необдуманные или непредусмотрительные действия.
B. Раннее появление хотя бы одного из следующих симптомов:
1) апатия,
2) инертность.
С. Ранняя утрата симпатии или эмпатии в виде хотя бы одного из следующих симптомов:
1) низкая отзывчивость в отношении нужд и чувств других людей,
2) сужение социальных интересов, утрата взаимопонимания или сердечности.
D. Раннее развитие персевераций, стереотипий или компульсий/ритуалов в виде хотя бы одного из следующих симптомов:
1) простые повторяющиеся движения,
2) сложные компульсии или ритуалы,
3) речевые стереотипии.
E. Гипероральность и изменения пищевого поведения в виде хотя бы одного из следующих симптомов:
1) изменения пищевых пристрастий,
2) переедание, чрезмерное потребление алкоголя или сигарет,
3) оральное манипулирование или потребление несъедобных объектов.
F. Нейропсихологический статус — хотя бы один из следующих симптомов:
1) дефицит регуляторных функций,
2) относительная сохранность эпизодической памяти,
3) относительная сохранность зрительно-пространственных функций.
III. Вероятный диагноз ЛВД с обязательным наличием следующих критериев:
А. Удовлетворяет критериям возможного ЛВД.
В. Значительное функциональное снижение (со слов ухаживающих лиц или по результатам клинической шкалы деменции (CDR)
или опросника функциональной активности (FAQ)).
C. Данные нейровизуализации (1 из 2 вариантов):
1) атрофия лобных и/или передневисочных отделов по данным МРТ или КТ,
2) гипоперфузия или гипометаболизм лобных и/или передневисочных отделов по данным ПЭТ или однофотонной эмиссионной
компьютерной томографии.
IV. Поведенческий вариант ЛВД с подтвержденной лобно-височной дегенерацией: критерий А в сочетании с критерием В или С:
А. Удовлетворяет критериям возможного и вероятного диагноза ЛВД.
В. Гистопатологическое подтверждение лобно-височной дегенерации по результатам биопсии или аутопсии.
С. Генетическое подтверждение: выявление известной патогенной мутации.
V. Критерии, исключающие диагноз ЛВД:
А. Клиническая картина более характерна для недегенеративного заболевания нервной системы или соматического заболевания.
В. Поведенческие нарушения лучше объясняются первично психиатрическим заболеванием.
С. Наличие биомаркеров, характерных для болезни Альцгеймера или иного нейродегенеративного заболевания (данный критерий
не исключает возможный диагноз ЛВД).
В набор двигательных нарушений, ассоциированных с ЛВД входят синдром бокового амиотрофического склероза (БАС) — деменции лобного типа, кортико-базальный синдром и синдром прогрессирующего надъядерного паралича. Двигательные нарушения могут как предшествовать развитию поведенческих, так и развиваться после них. Доля пациентов с когнитивными и поведенческими нарушениями, соответствующими ЛВД, среди лиц обратившихся в специализированные клиники нервно-мышечных заболеваний с типичной клиникой БАС составляет 15–20% (Murphy JM, Henry RG, 2017).
Сосудистое НКР
Сосудистым считается когнитивное нарушение, основной причиной которого является сосудистое поражение головного мозга.
Развитие сосудистой деменции происходит по двум основным сценариям:
- после перенесённого инсульта;
- при накоплении хронических сосудистых изменений без клинических и визуализационных признаков инсульта.
Факторы риска сосудистого НКР сходны с факторами риска цереброваскулярных заболеваний и включают: гипертонию, сахарный диабет, курение, ожирение, высокий уровень холестерина и гомоцистеина, факторами риска прогрессирования атеросклероза/артериосклероза; риск церебральной эмболии повышается при фибрилляции предсердий. Важными факторами риска являются церебральная амилоидная ангиопатия и аутосомная доминантная артериопатия с субкортикальными инфарктами и лейкоэнцефалопатией (CADASIL). При этом, коррекция факторов риска не обеспечивает существенного снижения риска развития деменции. По данным крупного исследования, долговременная терапия, направленная на снижение степени сосудистых изменений головного мозга у пожилых пациентов в амбулаторных условиях не приводила к уменьшению частоты развития деменции, темпа прогрессирования функциональных ограничений и смертности.
Перенесённый инсульт повышает риск развития деменции в 5 раз. В клинических исследованиях было показано, что СД возникает приблизительно у 25–30% пожилых, перенесших инсульт. Возможно не только непосредственное развитие когнитивных нарушений после инсульта, но и прогрессирование симптомов после острой фазы заболевания (Yang T, Sun Y, 2016).
Факторами риска развития постинсультной деменции являются:
- Характеристики пациента до развития инсульта (пожилой возраст, принадлежность пациента к монголоидной или негроидной расе, низкий уровень образования, сахарный диабет и фибрилляция предсердий).
- Характеристики инсульта (внутримозговое кровоизлияние, афазия, левополушарная локализация и множественные повторные инсульты)
- Осложнения инсульта (недержание мочи, спутанность сознания или судороги)
- Сниженный церебральный резерв (визуализационные признаки лейкоареоза, общая атрофия, атрофия медиальных отделов височной доли и отложение β — амилоида.
Диагностические критерии большого и малого сосудистого НКР по DSM-5
A. Соответствие критериям большого или малого нейрокогнитивного расстройства.
B. Клинические признаки соответствуют сосудистой этиологии:
1. Развитие когнитивного дефицита связано по времени с одним и более цереброваскулярными эпизодами.
2. Значимые нарушения отмечаются в сложных заданиях на внимание (включая, скорость обработки информации) и исполнительных функциях, опосредованных лобными долями.
C. Значимые для развития нейрокогнитивного дефицита признаки цереброваскулярного заболевания при сборе анамнеза, объективном исследовании и/или оценке результатов нейровизуализации.
D. Симптомы не имеют лучшего объяснения другим заболеванием головного мозга или системным заболеванием.
Вероятное сосудистое нейрокогнитивное расстройство диагностируется при соответствии одному из следующих утверждений; в противном случае, устанавливается диагноз возможного сосудистого нейрокогнитивного расстройства:
1. Клинические критерии подтверждаются данными нейровизуализации о значимом повреждении паренхимы головного мозга вследствие цереброваскулярного заболевания (подтверждённое визуализационными исследованиями).
2. Изменения нейрокогнитивного синдрома имеют временную связь с одним или более задокументированных цереброваскулярных эпизодов.
3. Одновременное наличие клинических и генетических (например, церебральная аутосомная доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией — CADASIL) признаков цереброваскулярного заболеваниями.
Возможное сосудистое нейрокогнитивное расстройство диагностируется, если случай соответствует клиническим критериям, а данные нейровизуализации не доступны, и не установлена временная связь динамики нейрокогнитивного синдрома с одним или более цереброваскулярных эпизодов.
Рисунок 6
STRIVE критерии классификации изменений головного мозга, вызванных заболеванием мелких артерий
Рисунок 7
МРТ пациента Ф. 75 лет с мультиинфарктной энцефалопатией и множественными лобарными гематомами
НКР, вызванное болезнью диффузных телец Леви
Большое и малое нейрокогнитивное расстройство, вызванное болезнью диффузных телец Леви
Диагностические критерии DSM-5
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Незаметное начало и постепенное прогрессирование.
C. Расстройство соответствует комбинации основных диагностических признаков и признаков подтверждающих диагноз вероятного или возможного нейрокогнитивного расстройства, вызванного болезнью диффузных телец Леви (БДТЛ).
Для диагноза вероятного большого или малого когнитивного расстройства, вызванного БДТЛ, у пациента должно быть два признака, подтверждающие диагноз в сочетании с одним или более основными признаками.
Для диагноза возможного большого или малого нейрокогнитивного расстройства, вызванного БДТЛ, пациенту достаточно иметь только один основной признак или не менее одного подтверждающего признака
1. Основные диагностические признаки:
a. Когнитивные флуктуации: выраженные колебания уровня внимания и скорости активизации.
b. Рецидивирующие зрительные галлюцинации, логичные, последовательные и детализованные.
c. Спонтанные (не индуцированные приёмом лекарств и действием других патологических факторов) симптомы паркинсонизма, развившиеся после когнитивных нарушений.
2. Подтверждающие диагностические признаки:
a. Соответствие критериям нарушений поведения во сне с быстрым движением глаз.
b. Выраженная чувствительность к нейролептикам.
D. Симптомы не имеют лучшего объяснения цереброваскулярным заболеванием, другим нейродегенеративным заболеванием, действием наркотиков, или другим психическим, неврологическим или системным заболеванием.
Эпизоды, включающие не менее трёх из четырёх признаков: сонливость в дневное время, сон в дневное время, продолжающийся более двух часов, длительные эпизоды задержки взгляда и эпизоды бессвязной речи более вероятно возникают у пациентов с ДТП, чем при БА (Ferman TJ, Smith GE, 2004)
Наряду с включёнными в критерии признаками, для болезни диффузных телец Леви характерны вегетативные нарушения (запоры, ортостатическая гипотензия и ортостатические синкопе, нарушения мочеиспускания и потоотделения), падения, нарушения сна. Эти расстройства сходны с профилем немоторных симптомов болезни Паркинсона, однако, в большинстве случаев более выражены.
В отличие от БА, при которой наиболее выраженным видом когнитивных нарушений, являются нарушения памяти, ДТЛ характеризуется ранним развитием нарушений внимания, исполнительных функций, зрительно пространственных нарушений; нарушения памяти возникают на более распространённых стадиях. В качестве ранних проявлений могут выступать затруднения при выполнении автомобилем (пациент теряется, неверно оценивает дистанции, не может остановиться перед запрещающими знаками и другими автомобилями) и рабочих обязанностей.
Для обследования пациентов больше подходят тесты, оценивающие зрительно-пространственные нарушения: копирование пятиугольников, тест с рисованием часов. В исследовании с последующей патогистологической верификацией диагноза (Tiraboschi P, Salmon DP, 2006) было показано, что отсутствие зрительно-пространственных нарушений на ранних стадиях, позволяет исключить ДТЛ с прогностической значимостью отрицательного результата 90%.
Распространённость ДТЛ в общей популяции пожилых 0,1–5%, 1,7–30,5% от общего количества деменций (по данным исследований с гистологическим подтверждением — 20–35%). Соотношение мужчин и женщин 1,5:1.
Большинство случаев ДТЛ характеризуется незаметным началом с постепенным прогрессированием. У отдельных пациентов, ретроспективно удаётся выявить продромальный период с развитием делириозных состояний (часто, спровоцированных соматическими болезнями или проведением операций). Большинство случаев начинаются на шестой — девятой декаде жизни (в среднем, в возрасте около 75 лет). По данным клинических наблюдений, средняя продолжительность жизни после установленного диагноза составляет 5–7 лет.
НКР, вызванное болезнью Паркинсона
Диагностические критерии DSM-5
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Нарушения развиваются у пациента с установленным диагнозом «болезнь Паркинсона».
C. Незаметное начало и постепенное прогрессирование.
D. Симптомы нейрокогнитивного расстройства не имеют лучшего объяснения другим заболеванием головного мозга или системным заболеванием.
Для диагноза вероятного большого или малого нейрокогнитивного расстройства, вызванного БП, необходимо одновременное соответствие пациента двум критериям. Диагноз возможного большого или малого нейрокогнитивного расстройства может быть установлен при соответствии одному из критериев:
1. Отсутствуют признаки смешанной этиологии (отсутствие признаков других нейродегенеративных заболеваний или цереброваскулярного заболевания или другого неврологического, психического или системного заболевания или иного состояния, которое может способствовать развитию когнитивных нарушений).
2. Развитие клиники болезни Паркинсона однозначно предшествует развитию нейрокогнитивного расстройства.
Установлено, что болезнь Паркинсона с деменцией (БПД) и деменция при болезни диффузных телец Леви (ДТЛ) имеют сходную патологическую основу и сходный профиль когнитивных нарушений у пациентов. Условным считается правило «одного года» — отрезка времени, на которое развитие паркинсонизма должно опережать развитие деменции, чтобы случай считался БПД (Aldridge GM, Birnschein A. 2018).
Факторами риска развития БПД являются возраст пациента ≥60 лет, высокая продолжительность и тяжесть паркинсонизма. Выделены генетические факторы риска: мутации в гене глюкоцереброзидазы (GBA) и генов, кодирующих отдельные формы α — синуклеина (SNCA). Деменция редко развивается в случаях БП, ассоциированных с мутацией генов, кодирующих паркин (PARK2). Быстрое развитие когнитивных нарушений при БП ассоциировано с ε2 и ε4 аллелями гена, кодирующего аполипопротеин E (ApoE), а также тау-белка, ассоциированного с микротрубочками (MAPT). Высокий риск когнитивных нарушений отмечен у пациентов с наследственно обусловленной низкой активностью катехоламин-О-метилтранферазы (Williams-Gray CH, Evans JR, 2009).
В развитии деменции у больных БП, наряду с недостаточностью дофамина, отмечается значение дефицита ацетилхолина, выраженность которого не меньше, чем при БА.
ДБП в отличие от ДТП медленнее прогрессирует, реже сопровождается зрительными галлюцинациями, чаще сопровождается тремором и асимметрией паркинсонизма. Флуктуации когнитивных нарушений более часто встречаются при ДТЛ.
НКР, вызванное травматическим повреждением головного мозга
Черепно-мозговая травма — основная причина смерти и инвалидизации пациентов в возрасте от 1 до 44 лет. Распространённость травм в развивающихся странах, выше, чем в развитых. По данным Thurman DJ, Alverson C, 2012, в США отдалённые последствия ЗЧМТ сохраняются у 2% населения.
Диагностические критерии DSM-5
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Убедительные признаки травматического повреждения головного мозга, как прямого воздействия, так и действие механизма «ускорение-замедление» на головной мозг и черепа с соблюдением не менее одного из следующих условий:
1. Потеря сознания.
2. Посттравматическая амнезия.
3. Спутанность сознания и дезориентированность.
4. Неврологические нарушения (признаки повреждения вещества головного мозга по данным нейровизуализации; вновь развившиеся эпилептические припадки; выраженное ухудшение диагностированного ранее заболевания с эпилептическими припадками; выпадение полей зрения; аносмия; гемипарез).
C. Нейрокогнитивное расстройство развивается непосредственно после полученной черепно-мозговой травмы или после восстановления сознания и сохраняется после истечения острого периода травмы.
Признаки, подтверждающие диагноз
Эмоциональные нарушения (раздражительность, напряжённость, тревожность, эмоциональная лабильность); изменения личности (расторможенность, апатия, подозрительность, агрессия); физические нарушения (головная боль, общая слабость, нарушения ночного сна, головокружение, шум в ушах и гиперакузия, светобоязнь, аносмия, снижение толерантности к алкоголю и психотропным препаратам); и, наиболее характерно для более тяжёлой ЧМТ, стойкие неврологические симптомы (судорожные припадки, гемипарез, зрительные нарушения, нарушения функции черепных нервов)
Тяжесть ЗЧМТ оценивается на момент получения травмы/первичного осмотра пациента как лёгкая, средней тяжести и тяжёлая в соответствии со следующими критериями.
Таблица 4
Критерии оценки тяжести черепно-мозговой травмы
| Характеристики травмы | Лёгкая ЗЧМТ | ЗЧМТ средней тяжести | Тяжёлая ЗЧМТ |
|---|---|---|---|
|
Потеря сознания |
<30 минуты
|
30 минут-24 часа
|
>24 часов |
|
Посттравматическая амнезия |
<24 часов |
24 часов — 7 дней |
>7 дней |
|
Дезориентированность или спутанность сознания при первичной оценке (Шкала ком Глазго) |
13–15 (не ниже 13 через 30 минут) |
9–12 |
3–8 |
Максимальная выраженность нарушений отмечается непосредственно после травмы. Нейрокогнитивные симптомы лёгкой ЗЧМТ сохраняются от нескольких часов до нескольких недель (не более 3-х месяцев); ухудшение состояния пациента требует исключения других механизмов повреждения мозга (сдавление внутримозговой гематомой).
Повторные лёгкие черепно-мозговые травмы могут приводить к более тяжёлым стойким последствиям. Это является проблемой спортивных единоборств. До повсеместного сопровождения боксёрских поединков рефери (конец 1940-х годов) и врачом (1979), часто развивалось стойкое нарушения активности и координации движений спортсменов, получавших повторные травмы (punch drunk — досл. «оглушённый ударом», а с 1937 года — dementia pugilistica «деменция боксёров»). Возникшие нарушения могли не прогрессировать до окончания карьеры, но в ряде случаев — отмечалось выраженное ухудшение. Это приводило к существенному уменьшению продолжительности карьеры и количества поединков до её окончания.
У небольшой доли пациентов развивается синдром повторного сотрясения (second-impact syndrome — SIS) — диффузный отёк головного мозга после повторных травм. Чаще возникает у спортсменов на фоне симптомов полученного ранее сотрясения головного мозга.
В 1998 году было описано 17 случаев, в 12 из них описание не было полным. В работе 2013 года не было выделено состояний, которые можно однозначно рассматривать как факторы риска SIS.
В настоящее время, в соответствии с правилами вида спорта «Бокс» (утв. приказом Министерства спорта РФ от 23 ноября 2017 г. N 1018), участники соревнований реже одного раза в 2 года проводят МРТ головного мозга; если, по мнению Врача или уполномоченных официальных лиц, у боксера проявляются явные признаки хронического сотрясения мозга во время боя, его лицензия отзывается, даже если при медицинском обследовании не обнаруживаются признаки травматической энцефалопатии.
Последствия травм, в том числе, протекающие с нейрокогнитивными нарушениями, крайне разнородны (от случаев с практически полным восстановлением до персистирующего вегетативного состояния). Клиника находится зависит от стадии, локализации и распространённости органических поражений головного мозга.
НКР, вызванное ВИЧ-инфекцией
ВИЧ проникает в нервную систему и может быть выделен из спинномозговой жидкости спустя несколько дней после инфицирования. В пределах мозговой ткани, ВИЧ проявляет тропность к макрофагам (в противоположность тропности к Т-лимфоцитам в крови) и астроцитам. Периваскулярные макрофаги и связанные с ними клетки являются местом развития инфекционных изменений в головном мозге; являются источником постоянной продукции токсических веществ, что приводит к нарушению функции и развитию когнитивных нарушений.
Большая распространённость (60–80% пациентов) когнитивных нарушений у пациентов с ВИЧ была установлена в самом начале эпидемии, в 1986 году был предложен термин «СПИД-дементный комплекс». В 1991 году Американская академия неврологии предложила выделить две категории когнитивных нарушений при ВИЧ-инфекции: 1. ВИЧ-ассоциированная деменция; 2. легкая форма с минимальными когнитивными или двигательными нарушениями. Однако эти термины не отражали в полной мере, весь спектр неврологических проявлений ВИЧ-инфекции и в 2007 году появилась альтернативная классификация, включающая три категории:
1) бессимптомное нейрокогнитивное расстройство (АНР);
2) ВИЧ-ассоциированное лёгкое нейрокогнитивное расстройство (ЛНР);
3) ВИЧ-ассоциированная деменция (ВАД). Так же были сформулированы диагностические критерии нейрокогнитивных расстройств – критерии Фраскати, предложены диагностические шкалы, оценивающие семь когнитивных процессов.
Таблица 5
Критерии диагностики ВИЧ-ассоциированных когнитивных нарушений
| Вид | ВИЧ-ассоциированные когнитивные нарушения |
|---|---|
|
БНР |
ВИЧ-ассоциированное бессимптомное нейрокогнитивное расстройство Когнитивные нарушения вовлекают как минимум два когнитивных домена (оценки результатов нейропсихологического теста отличаются норм не менее чем на 1 стандартное отклонение) Когнитивные нарушения не оказывают влияния на повседневную активность пациентов. |
|
ЛНР |
ВИЧ-1-ассоциированное лёгкое нейрокогнитивное расстройство Когнитивные нарушения вовлекают как минимум два когнитивных домена (оценки результатов нейропсихологического теста отличаются норм не менее чем на 1 стандартное отклонение) Когнитивные нарушения оказывают, как минимум, лёгкое влияние на повседневную активность пациентов. |
|
ВАД |
ВИЧ-1-ассоциированная деменция (ВАД) Выраженные когнитивные нарушения вовлекают как минимум два когнитивных домена (оценки результатов нейропсихологического теста отличаются норм не менее чем на 2 стандартных отклонения) Когнитивные нарушения оказывают выраженное влияние на повседневную активность пациентов. |
Критерии применимы только в случае отсутствия других причин, объясняющих развитие когнитивных нарушений (оппортунистические инфекции, инсульт, метаболическое или токсическое воздействие на головной мозг) и состояний, которые могут изменять результаты нейропсихологических тестов (употребление наркотиков, перенесённая ЧМТ или тяжёлое психическое заболевание).
Сопутствующие поведенческие нарушения чаще всего представлены апатией, снижением мотивации. У пациентов с ВИЧ-ассоциированной деменцией распространены раздражительность, бессонница, снижение массы тела, беспокойство и тревожность. Часть этих симптомов может быть связана с депрессией, в течение которой у пациентов с ВИЧ редко встречаются дисфория, приступы рыдания и жалобы на грустное настроение.
Неврологические нарушения, распространённые среди пациентов с ВАД включают: замедленность движений (по результатам теппинг-теста), нарушение саккадических движений глаз, нарушение плавности движений, особенно нижних конечностей, нарушение содружественных движений рук при ходьбе — дисдиадохокинез, гиперрефлексия и лобные знаки, такие как хватательный рефлекс, дистантно-оральный и глабеллярный рефлекс.
Ввиду того, что пациенты с ВИЧ редко активно предъявляют когнитивные жалобы, предлагается проведение скрининга когнитивных нарушений. Для этого используются краткие инструменты оценки и опросники. Приблизительный набор вопросов:
- Часто ли у вас бывают случаи потери памяти (например, вы забываете
значительные события, даже самые недавние, назначенные встречи и
т. д. )? - Считаете ли вы, что стали медленнее думать, строить планы или решать проблемы?
- Бывают ли вам трудно сосредоточиться (когда разговариваете с кем-то, читаете книгу или смотрите фильм)?
Считается, что у ВИЧ-инфицированного пациента имеются когнитивные нарушения, если он ответил «да» на один или более вопросов. В этом случае требуется проведение более детальной оценки.
НКР, вызванное действием лекарственных или наркотических веществ;
Диагностические критерии DSM-5
НКР, вызванное действием лекарственных или наркотических веществ
Большое или малое нейрокогнитивное расстройство, вызванное действием лекарственных или наркотических веществ
Диагностические критерии
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Нейрокогнитивные нарушения нельзя объяснить исключительно с делирием, и они сохраняются дольше обычной длительности интоксикации или последствий отмены.
C. Продолжительность и выраженность действия предполагаемого в качестве причины наркотика или лекарственного препарата достаточны, что вызвать нейрокогнитивные нарушения.
D. Течение нейрокогнитивного дефицита соответствует времени приёма наркотика или лекарственного препарата и развития синдрома их отмены (дефицит остаётся стабильным или уменьшается после абстиненции).
E. Нейрокогнитивное расстройство не вызвано другим соматическим заболеванием или не имеет лучшего объяснения другим психическим заболеванием.
В DSM-5 выделяется:
- Алкогольное (большое нейрокогнитивное расстройство), неамнестический-конфабуляторный тип
- Алкогольное (большое нейрокогнитивное расстройство), амнестический-конфабуляторный тип
- Алкогольное (малое нейрокогнитивное расстройство)
- Вызванное употреблением летучих веществ ингаляционного действия (ЛВНД) — «ингалянтов» (большое нейрокогнитивное расстройство)
- Вызванное употреблением летучих веществ ингаляционного действия (ЛВНД) — «ингалянтов» (малое нейрокогнитивное расстройство)
- Вызванное приёмом седативных, снотворных или анксиолитических препаратов (большое нейрокогнитивное расстройство)
- Вызванное приёмом седативных, снотворных или анксиолитических препаратов (малое нейрокогнитивное расстройство)
- Вызванное приёмом других (или неизвестных) препаратов (большое нейрокогнитивное расстройство)
- Вызванное приёмом других (или неизвестных) препаратов (малое нейрокогнитивное расстройство)
Категория «другие наркотические вещества» используется для наркотиков, не входящих в какой-либо из классов; а в случаях, когда причиной нарушений предполагается неустановленное лекарственное вещество, классовая принадлежность которого неизвестна, используется группа «неизвестное наркотическое вещество»
Дополнительно указать:
Персистирующее нейрокогнитивное расстройство, сохраняющееся после длительного периода абстиненции.
Диагностические признаки
Большое или малое нейрокогнитивного расстройство рассматривается как вызванное приёмом наркотических веществ/лекарственных препаратов, если оно сохраняется после обычной продолжительности токсического действия и острого синдрома отмены вызвавшего его соединения (Критерий B). В начале, эти проявления могут соответствоать медленному восстановлению функция головного мозга после периода длительного использования, улучшение нейрокогнитивных функций, в то время как, визуализационные признаки нарушений могут сохраняться в течение нескольких месяцев. Если расстройство продолжается в течение длительного периода или становится стойким, это нужно указывать. Необходимо наличие данных о том, что вид и характер использование предполагаемого вещества вызывают наблюдаемые нарушения (Критерий C).
НКР, вызванное болезнью Гентингтона
Диагностические критерии DSM-5
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Незаметное начало и постепенное прогрессирование.
C. Клинический диагноз болезни Гентингтона или риск развития болезни Гентингтона по данным семейного анамнеза или генетического тестирования.
D. Симптомы нейрокогнитивного расстройства не имеют лучшего объяснения другим заболеванием головного мозга или системным заболеванием.
Симптомы болезни Гентингтона
Неврологические
Хорея — быстрые внезапные нестереотипные движения, вовлекающие лицо, туловище и конечности
Дистония — длительные, стойко сохраняющиеся патологические позы, отмечаются чаще всего в руках при различных видах сопутствующей активности, например, при ходьбе.
Замедление движений глаз
Оживление глубоких рефлексов
Нарушения ходьбы
Миоклонус (редко)
Паркинсонизм (на поздних стадиях)
Психиатрические
Апатия
Раздражительность
Депрессия
Галлюцинации
Агрессия
Тревожность
Расторможенность
Паранойя
Когнитивные
Неспособность к формированию суждений
Негибкость мышления
Неспособность схватывать суть происходящего
Нарушение концентрации внимания
Снижение памяти
Подкорковая деменция
Снижение массы тела и кахексия
Патогенез симптомов окончательно не установлен, наиболее вероятной причиной являютя энергозатраты на непроизвольные движения. Установлена большая выраженность кахексии у пациентов с большим количеством повторов ЦАГ.
Атипичные симптомы
Мозжечковая атаксия туловища и конечностей (у более молодых пациентов), паркинсонизм (у более пожилых пациентов).
Клинические признаки ювенильной хореи Гентингтона
Ригидрость
Брадикинезия
Миоклонии
Спастичность
Мозжечковые симптомы
Минимальная выраженность хореи
Когнитивные и поведенческие нарушения
Эпилепсия
Данные нейровизуализации
Атрофия хвостатого ядра — отсутствие нормального выпячивания головки хвостатого ядра в полость бокового желудочка на поздних стадиях, прогрессирующее уменьшение толщины коры головного мозга.
Клиническое прогрессирование заболевания
Вне зависимости от возраста начала, БГ характеризуется хроническим медленно прогрессирующим течением, в котором условно выделяется три стадии:
Ранняя стадия — пациенты на ранней стадии БГ обычно сохраняют независимость и способны самостоятельно выполнять повседневные дела, могут продолжать работать и водить автомобиль. На этой стадии появляются лёгкие непроизвольные движения, нарушения координации движений, трудности при выполнении сложных видов умственной активности. У пациентов появляются раздражительность, расторможенность или депрессия. Могут отмечаться замедления произвольных движений глаз, в особенности у молодых пациентов.
Промежуточная стадия — пациенты начинают испытывать затруднения в работе, управлении автомобилем, ведении личных счетов. В большинстве случаев, пациентам требуется некоторая помощь при приёме пищи, одевании, уходе за собой. Увеличивается выраженность хореи и других непроизвольных движений; нарушения ходьбы и равновесия могут приводить к падениям. Возникают нарушения глотания и снижение массы тела.
Поздняя стадия — медленное, но неуклонное ухудшение когнитивных и двигательных функций вызывает выраженную инвалидизацию и повышает риск ранней смертности. Сохранные активные движения неловкие, высокоамплитудные, могут приводить к падениям и травмам конечностей. Большинство пациентов прикованы к постели. При развитии дисфагии может потребоваться переход на зондовое питание.
Продолжительность жизни пациентов на этой стадии зависит от качества ухода. Основной причиной смерти являются осложнения: пролежни, пневмония, мочевая инфекция.
Диагностика
Диагноз БГ основывается на типичной клинической картине, семейном анамнезе заболевания (если доступен) и результатах генетического исследования.
Нейровизуализация используется для исключения других структурных изменений головного мозга.
Анамнестических указаний на больных родственников нет лишь у 8% с генетически подтверждённой БГ. Это может быть связано с внезапной смертью родственников. При сборе семейного анамнеза выявляются лица с психическими нарушениями, лица совершившие суицид.
Чувствительность генетического тестирования составляет 98,8%, а специфичность — 100%, что позволяет подтвердить формы с атипичными симптомами.
Результаты тестирования необходимо учитывать при планировании семьи.
Проведение генетического тестирования показано взрослым пациентам с симптомами БГ, вне зависимости от семейного анамнеза заболевания.
Лечение
Болезнь-модифицирующее лечение БГ не разработано.
Для контроля двигательных симптомов используются недоступные в России тетрабеназин дейтетрабеназин — синтетические производные бензохинолизина.
Препаратами второго ряда являются нейролептики. В случае тяжёлых проявлений хореи — выбирается один из мощных типичных нейролептиков — галоперидол, флуфеназин или хлорпромазин. У пациентов с более лёгкими нарушениями предпочтительны атипичные нейролептики — оланзапин, рисперидон или арипипразол.
Для купирования психотических нарушений, в отсутствии функционально значимой хореи, назначается кветиапин. К альтернативным препаратам относятся оланзапин и рисперидон.
НКР, вызванное прионным заболеванием
Прионные заболевания — нейродегенеративные заболевания с длительным инкубационным периодом и неуклонным прогрессированием с момента появления первых симптомов
к настоящему времени описано 5 видов прионных заболеваний:
- куру,
- болезнь Крейтцфельдта-Якоба (БКЯ),
- вариантная болезнь Крейтцфельдта-Якоба (вБКЯ),
- синдром Герстманна-Штреусслера-Шейнкера (ГШШ),
- фатальная семейная бессонница (FFI).
Около 90% случаев прионных заболеваний — болезнь Крейтцфельдта-Якоба.
- Заболеваемость составляет около 1 случая на 1 000 000.
- Средний возраст начала заболевания — 56–62 года. При этом, есть малочисленные описания развития заболевания у молодых людей и лиц, старше 80 лет.
- Факторами риска являются семейный анамнез (ОШ 19,1) и психотические нарушения в анамнезе (ОШ 9,9).
- Получены данные о связи риска развития заболевания с проживанием в отдельных географических регионах.
- Пациенты с вариантной (<1%, точных данных нет, описано менее 300 случаев) и ятрогенной формами БКЯ (<1%), как правило, моложе.
- Средний возраст развития семейной формы БКЯ (5–15%) лишь незначительно младше, чем у других форм.
Диагностические критерии DSM-5
A. Случай соответствует критериям большого или малого когнитивного расстройства.
B. Незаметное начало и быстрое прогрессирование нарушений.
C. Наличие характерных для прионных заболеваний двигательных нарушений, таких как миоклонус или атаксия или выявление биомаркеров
D. Симптомы нейрокогнитивного расстройства не имеют лучшего объяснения другим заболеванием головного мозга или системным заболеванием.
Рисунок 8
Патология
- Губчатые изменения вещества головного мозга — формирование небольших вакуолей размером 20–50 мкм, при электронной микроскопии — вакуоли располагаются между нейронами.
- Утрата синаптических связей
- Гибель нейронов и атрофия вещества мозга без сопутствующих признаков воспаления
- Накопление прионного белка
Рисунок 9
Патогистологические изменения ткани мозга при болезни Крейтцфельдта-Якоба
|
Микрофотография препарата мозга пациента с классическим вариантом БКЯ с признаками мелких вакуолей сером веществе коры головного мозга (низкое разрешение) |
Микрофотография препарата мозга пациента с классическим вариантом БКЯ с характерной для заболевания вариабельностью размеров вакуолей (высокое разрешение) |
Микрофотография препарата, окрашенного для выявления прионного белка при помощи иммунопероксидазы. выявляет диффузный и гранулярный синаптический характер распределения изменений (среднее разрешение) |
|
|
||
Рисунок 10
Динамика МР-картины прионного заболевания у мужчины 62 лет,
верхний ряд снимков — май 2017, нижний — октябрь 2017
Специального лечения прионных болезней не разработано.
В большинстве случаев, пациенты с прионным заболеваниями погибают в течение года с момента начала заболевания; средняя продолжительность жизни — 6 месяцев.
НКР, вызванное другими заболеваниями
Причинами деменции, не имеющими специального раздела в классификации DSM-5, являются
- структурные изменения (первичные или метастатические опухоли, субдуральные гематомы, медленно-прогрессирующая обструктивная или нормотензивная гидроцефалия);
- гипоксия, связанная гипоперфузией при заболеваниях сердца;
- последствия эндокринных нарушений (гипотиреоз, гиперкальциемия, гипогликемия);
- нарушения питания (дефицит тиамина — витамина В1 или никотиновой кислоты;
- инфекционные заболевания (нейросифилис, токсоплазмоз, криптококкоз);
- иммунно-опосредованные заболевания (височный артериит, системная красная волчанка, паранеопластический энцефалит);
- печёночная и почечная недостаточность,
- метаболические нарушения (болезнь Куфса — цероид-липофусциноз, адренолейкодистрофия, метахроматическая лейкодистрофия и другие болезни накопления взрослого и детского возраста) и
- другие неврологические заболевания (эпилепсия, рассеянный склероз).
Доказательством причинной связи этих состояний с развитием деменции служит временная связь начала и соответствие тяжести течения основного заболевания динамике когнитивного дефицита.
НКР вследствие действия нескольких причин
Ввиду наиболее высокой распространённости болезни Альцгеймера и цереброваскулярных заболеваний, наиболее часто встречается их сочетание, а также сочетание каждого вида патологии с более редкими типами деменции.
Оценить вклад факторов в каждом отдельном случае крайне сложно, ввиду отсутствия абсолютной патологической значимости сосудистых и альцгеймеровских изменений.
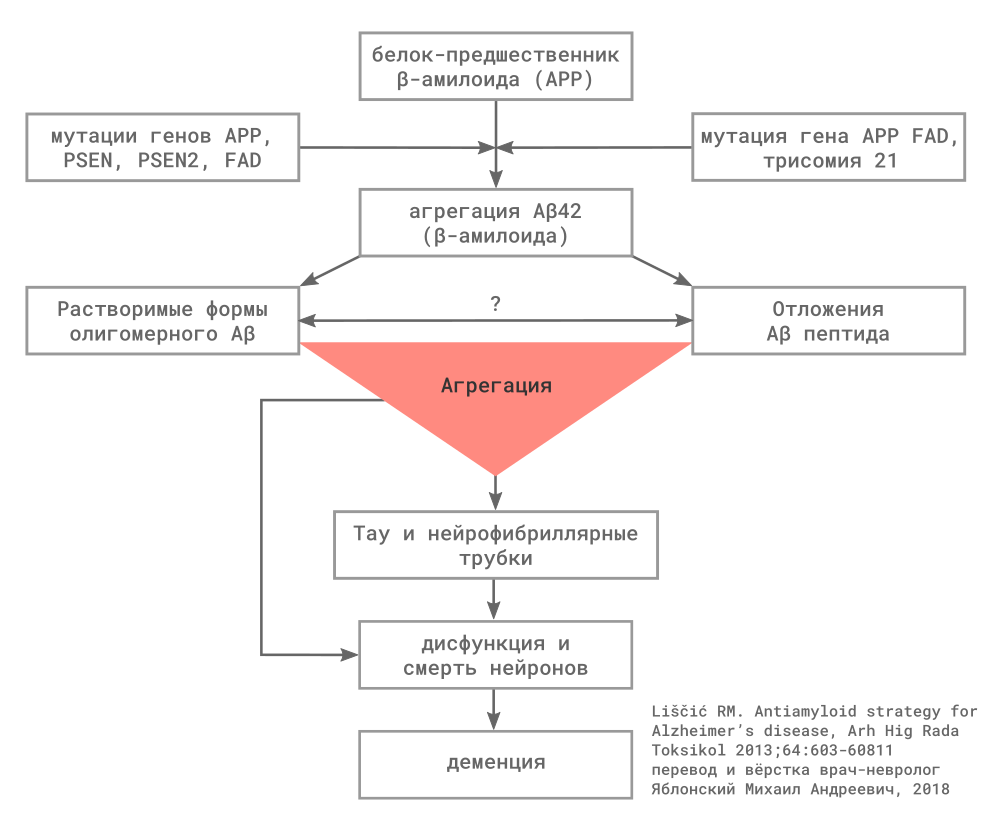
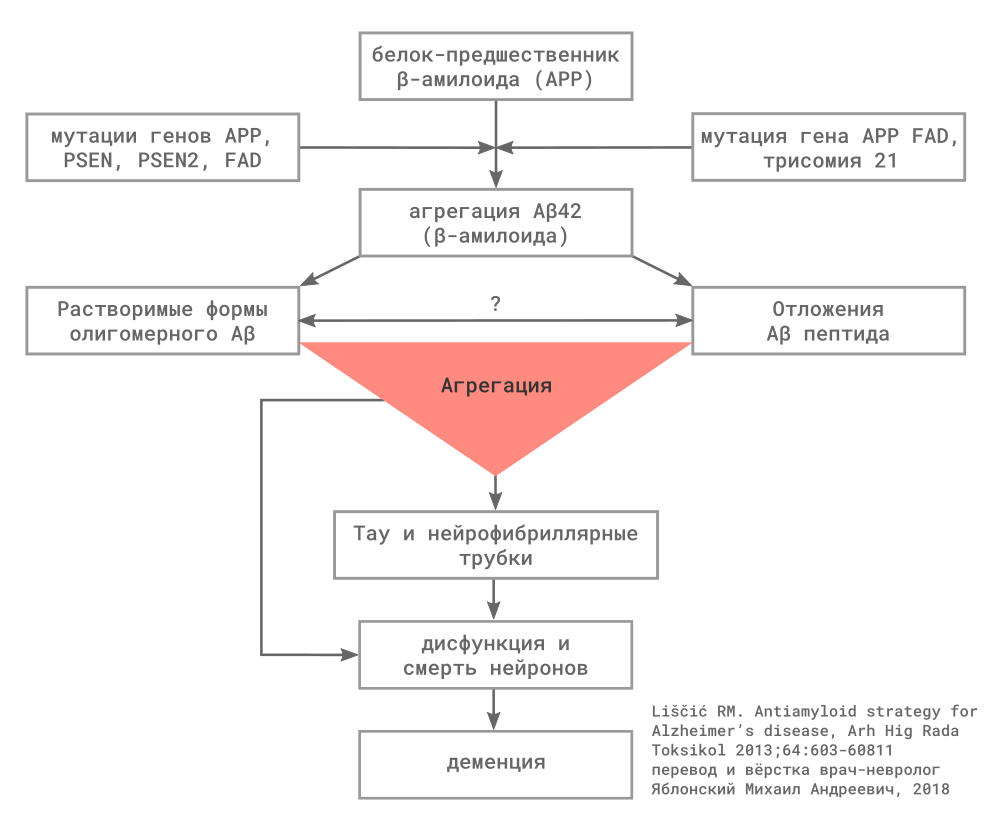
Рисунок 11
Взаимоотношение сосудистых и других типов нейрокогнитивных нарушений
Неуточнённое НКР
Раздел используется в случаях, когда при обследовании не удаётся установить причину нарушений.
Приложение 1 Основные характеристики отдельных типов деменции
Трансформация УКР в деменцию
При проведении мета-анализа 41 когортного исследования, было установлено, что среднегодовая частота трансформации УКР в деменцию составляет 5–10%, при этом, у большинства пациентов, УКР никогда не трансформируется в деменцию.
Нейровизуализация
Результаты КТ и МРТ головного мозга в большинстве случаев не дают однозначного ответа о типе деменции: болезни Альцгеймера и сосудистой деменции, а также не позволяют разделить пациентов с деменцией от пациентов без деменции. Основной задачей визуализации является исключение потенциально устранимых причин когнитивных нарушений: опухолей, субдуральных гематом, нормотензивной гидроцефалии. Оценка выраженности сосудистых изменений не имеет большого значения, ввиду их высокой распространённости и сочетании с патологическими процессами приводящими к более редким типам деменции. Проведение МРТ или КТ головного мозга в ряде случаев обеспечивает информацией родственников и близких пациента в пользу органической природы ухудшения состояния (атрофия, последствия микроинфарктов, лейкоареоз).
Магнитно-резонансная томография
Атрофия гиппокампа
Атрофия гиппокампа является фактором риска развития когнитивных нарушений и деменции при нормальном старении и трансформации амнестического УКР в БА. Частота выявления атрофии гиппокампа, оцененная в поперечном исследовании и по данным мета-анализа у больных с БА составляет 4,66% в год, а в контрольной группе — 1,41%. Атрофия гиппокампа и серого вещества височных долей часто выявляются у здоровых пожилых людей без когнитивных нарушений, но их выявление — прогностический фактор развития деменции и смерти в дальнейшем (Ikram MA, Vrooman HA, 2010).
Компьютерная томография
Несмотря на меньшую чувствительность КТ к дегенеративным изменениям, по сравнению с МРТ, исследование позволяет достаточно точно выявить внутричерепные травматические изменения и их последствия, оценить характер и выраженность гидроцефалии. Исследование требует меньше времени, что критично важно для пациентов с нарушениями поведения. КТ может использоваться для пациентов с кардиостимулятором и недавно выполненным стентированием артерий, что важно для обследования лиц с послеоперационным делирием.