Целью вторичной профилактики является предотвращение повторного ишемического инсульта или повторной ТИА.
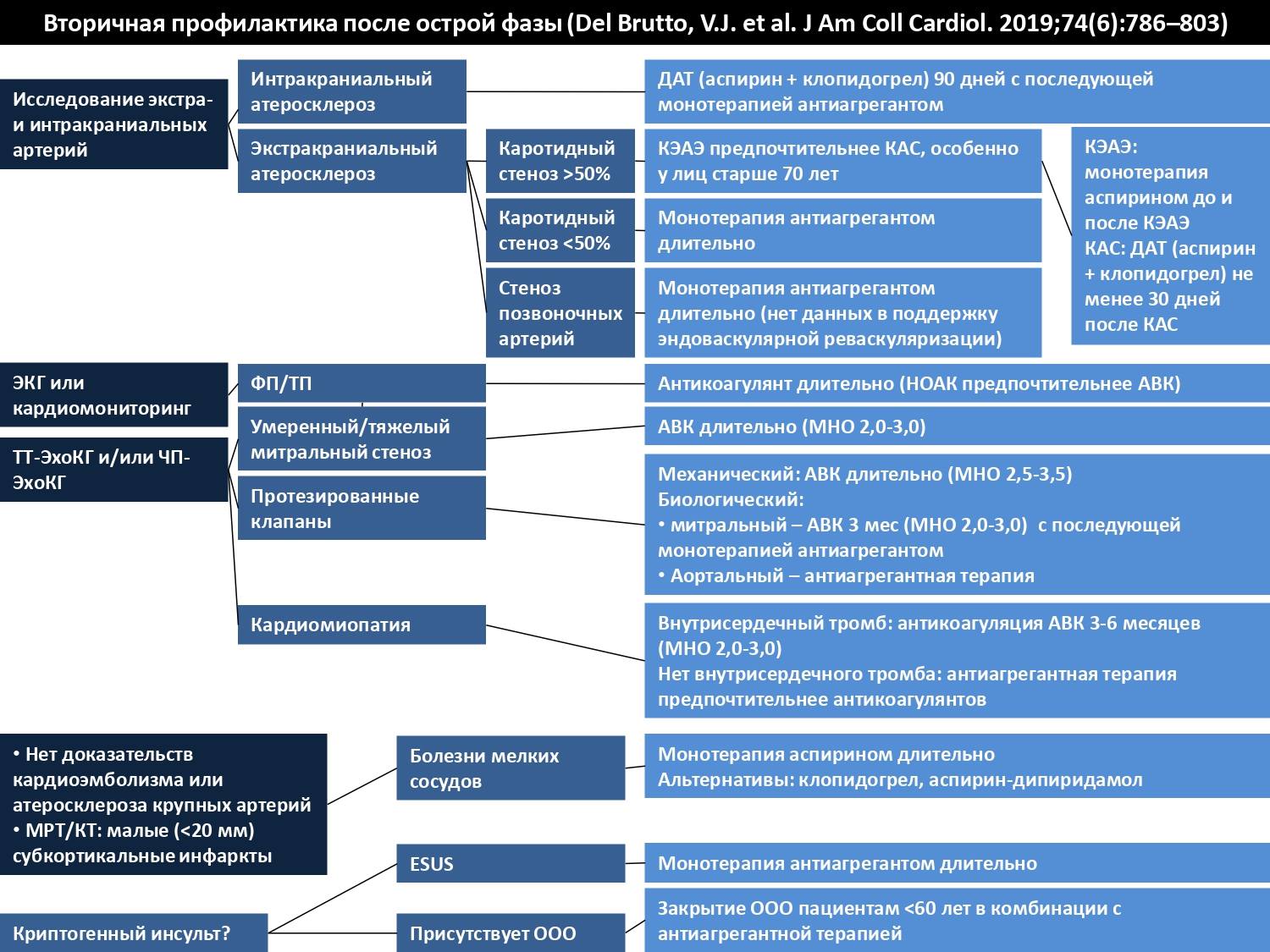
Антитромботическая терапия
Каждый пациент, перенесший инсульт/ТИА должен получать антитромботическую терапию. Выбор антитромботической терапии зависит от причины ишемического инсульта или ТИА. В связи с этим определение патогенетического подтипа ишемического инсульта или ТИА является принципиальным вопросом.
Ранняя вторичная профилактика
Целью ранней вторичной профилактики является предотвращение повторного инсульта в 24–48 ч от острого церебрального ишемического события. Риск развития повторного инсульта в первую неделю составляет: при кардиоэмболическом патогенетическом подтипе примерно 2,8%; при атеротромботическом – 8,1%; при лакунарном – 3,0%.
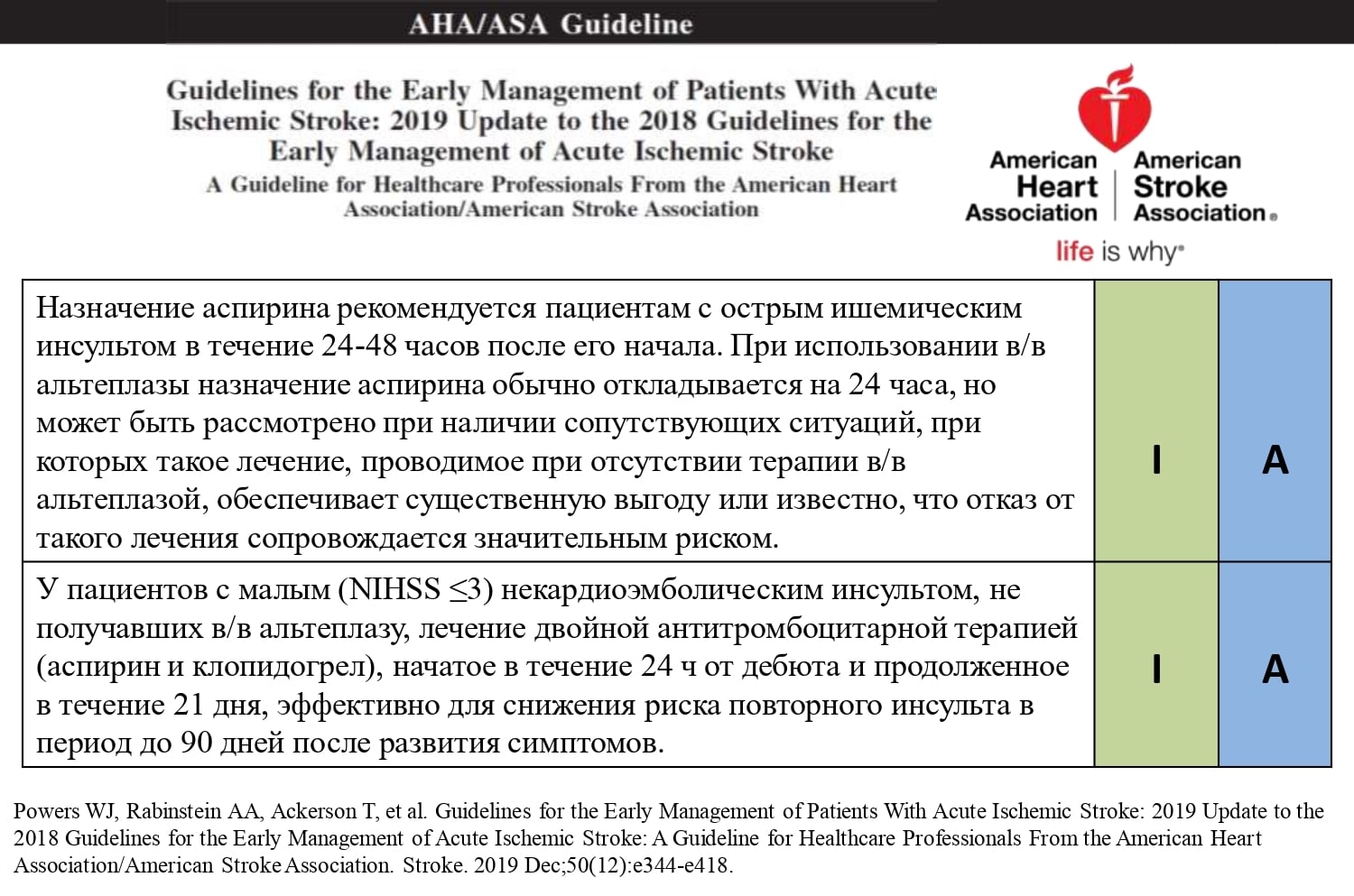
В случае возникновения инсульта на фоне приема Aspirin, рекомендовано в первые 24 часа назначить нагрузочную дозу Ticagrelor 180 мг, со вторых суток перейти на режим 90 мг дважды в день в течение как минимум 90 дней. Целесообразно через 90 дней отменить Ticagrelor и перейти на Сlopidogrel 75 мг в сутки.
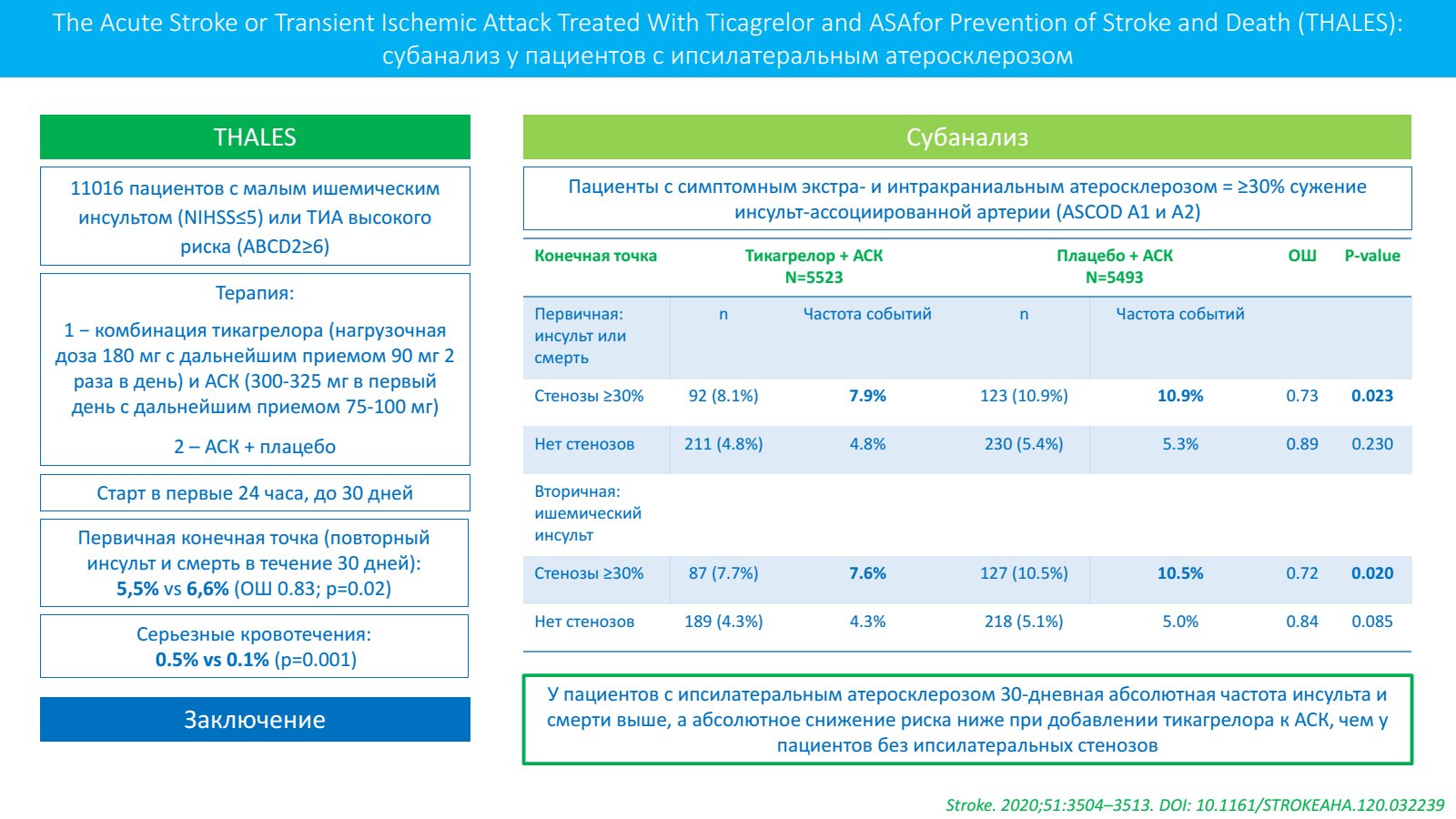
В случае возникновения инсульта на фоне приема Aspirin, увеличение дозировки последнего нецелесообразно.
В случае если планируется выполнение декомпрессионной трепанации черепа, назначение антитромботической терапии откладывается.
Незамедлительное назначение антикоагулянтов в лечебных дозах всем пациентам, с целью предотвращения повторных инсультов не рекомендуется.
Постоянная инфузия Heparin с поддержанием АЧТВ 1,5–2,0 нормы может быть полезна у пациентов с ИИ имеющих:
- кардиальные источники эмболии с высоким риском рецидива (искусственные клапаны сердца, инфаркт миокарда с внутрисердечным тромбом, фибрилляция предсердий с верифицированным тромбом в левом предсердии, внутрисердечные тромбы или инфаркт миокарда в течение последних 4 недель);
- симптомный экстракраниальный или интракраниальный стеноз с рецидивирующими ТИА или ИИ по типу «крещендо»;
- окклюзия базилярной артерии до или после внутриартериального тромболизиса или тромбоэкстракции;
- верифицированные коагулопатии.
- диссекции мозговых артерий.
- тромбоз венозных синусов, с рецидивирующими ТИА/ИИ.
Во время лечения Heparin необходимо не реже 2 раз в неделю исследовать клинический анализ крови с подсчетом тромбоцитов (вследствие риска развития гепарин-индуцированной тромбоцитопении).
В связи с высоким риском кровотечения (в т. ч. развития симптомной геморрагической трансформации инфаркта головного мозга), долгосрочная антикоагуляция НФГ не должна использоваться, если у пациента верифицировано:
- неконтролируемая гипертония;
- тяжелый неврологический дефицит (NIHSS > 20);
- большой объем инфаркта головного мозга (более 1/3 бассейна средней мозговой артерии, обширный инфаркт мозжечка);
- расслоение аорты;
- инфекционный эндокардит;
- алкогольная зависимость;
- болезнь печени с развитием печеночной недостаточности;
- повреждения с кровотечением;
- злокачественная опухоль;
- ретинопатия с высоким риском кровотечения;
- выраженные микрососудистые изменения головного мозга;
- аневризма мозговой артерии;
- предыдущее спонтанное церебральное кровоизлияние;
- геморрагический диатез (например, при коагулопатии, тромбоцитопении).
Другие антитромботические препараты в качестве средства вторичной профилактики инсульта в первые 48 часов, как правило, не назначаются (исключение – раннее стентирование).
Кардиоэмболический инсульт
Фибрилляция предсердий
Около 30% криптогенных инсультов происходят на фоне неверифицированной пароксизмальной формы фибрилляции предсердий. С целью диагностики скрытого нарушения ритма по типу фибрилляции предсердий, желательно проведение как минимум 72-часового холтеровского мониторинга ЭКГ, для более точной диагностики оптимален пролонгированный мониторинг ЭКГ (накладные ЭКГ-мониторы (patch-monitors), наружные петлевые регистраторы (external loop recorders)).
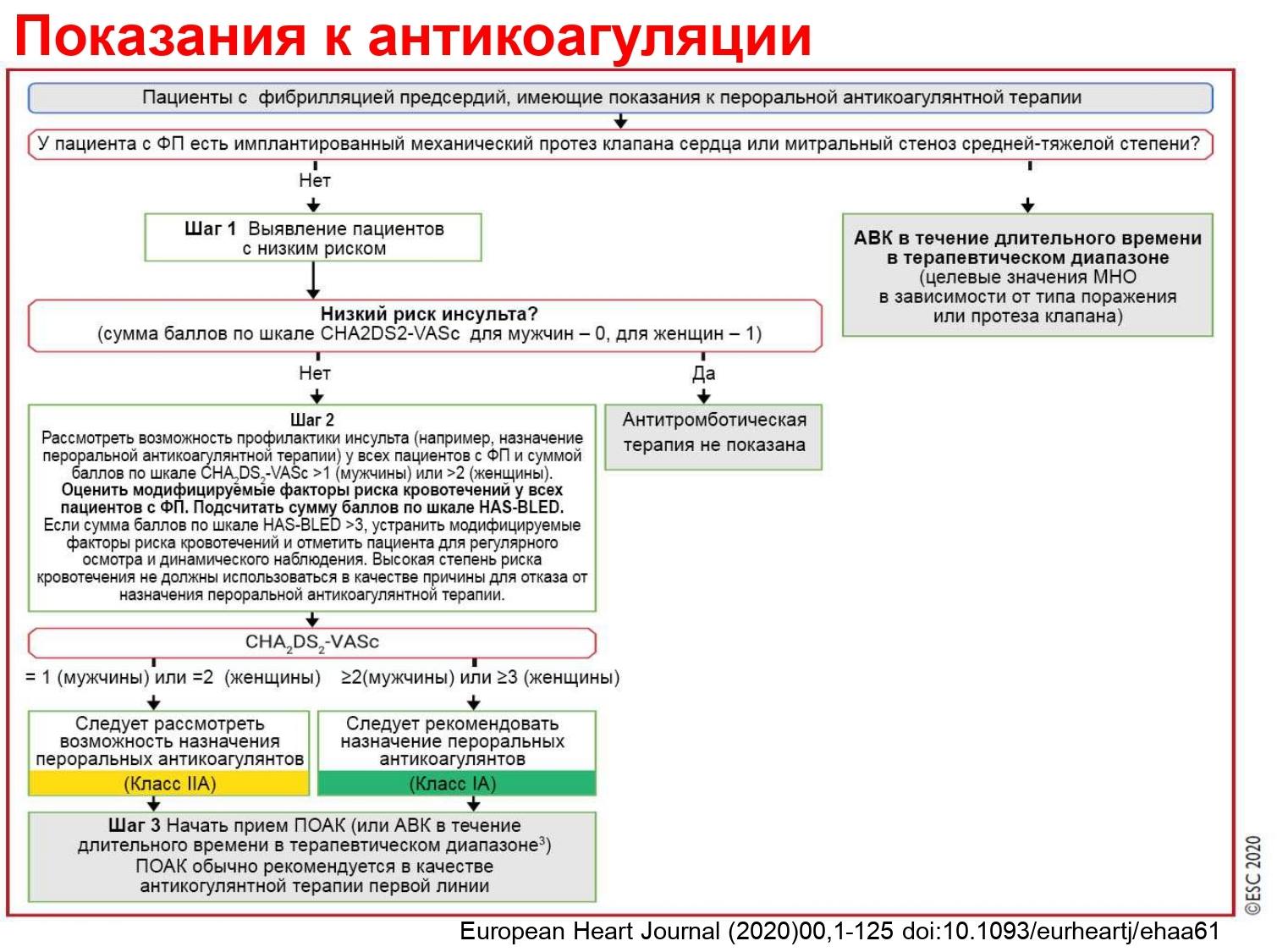
Пациентам, с впервые выявленной неклапанной фибрилляцией предсердий предпочтительнее назначение одного из НОАК (dabigatran, apixaban или rivaroxaban), чем антагонистов витамина К.
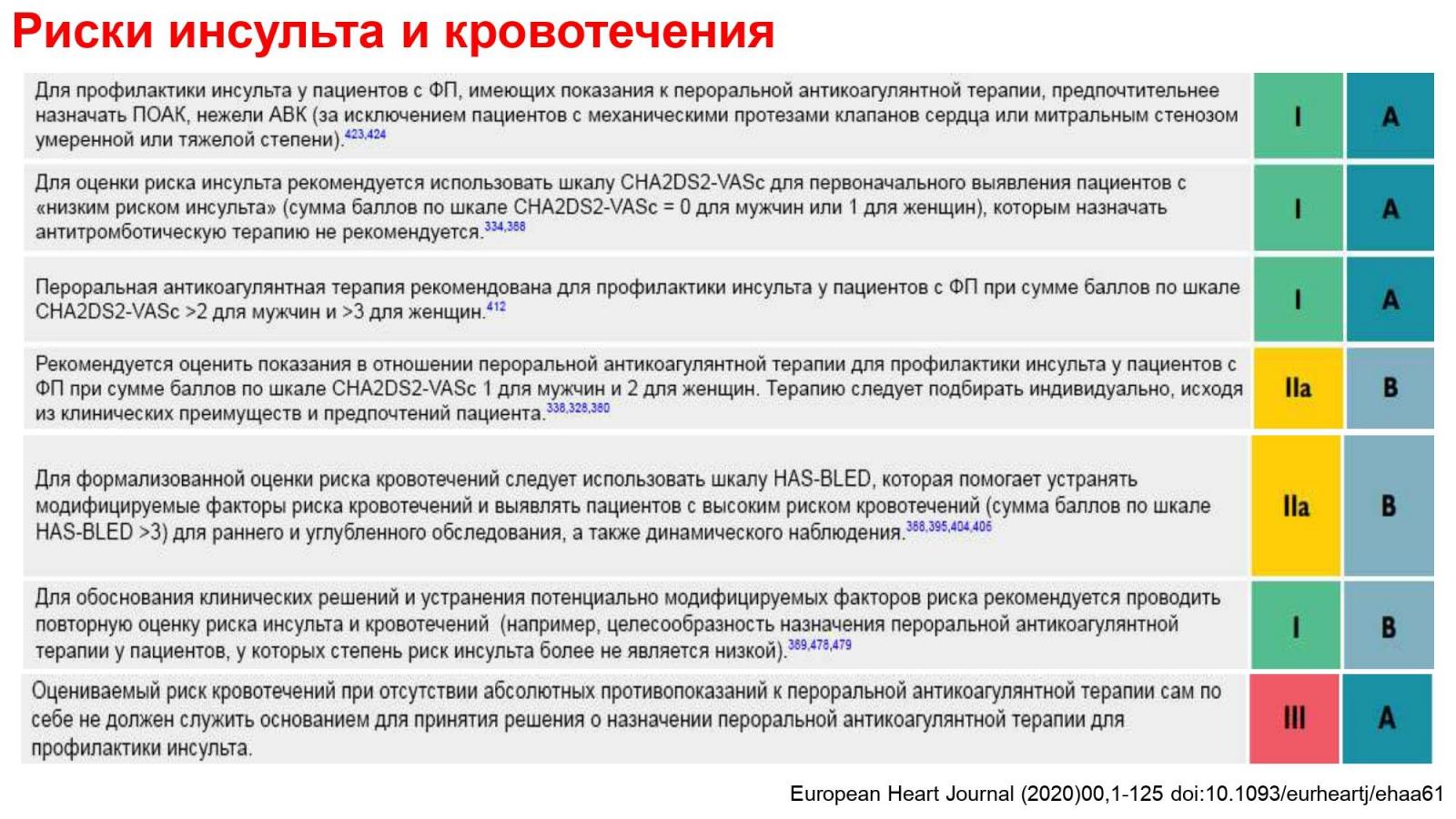
Пациентам с клапанной (умеренный или тяжелый митральный стеноз ревматической этиологии, механические протезы клапанов сердца или биологические протезы в первые 6 месяцев после установки) фибрилляцией предсердий, показан прием Warfarin, с необходимостью титрования дозы с поддержанием целевого значения МНО 2,5 (интервал 2,0 – 3,0) – для искусственного клапана в аортальной позиции, МНО 3,0 (2,5 — 3,5) – для искусственного клапана в митральной позиции. Назначение НОАК таким пациентам противопоказано.
Перед началом терапии НОАК необходимо оценить риск развития повторного инсульта/системной тромбоэмболии (шкала CHA2DS2-VASC, риск кровотечения (целесообрано выявление модифицируемых факторов риска и их коррекция, высокий риск по шкале HAS-BLED не является противопоказанием для назначения НОАК), и функцию почек (рассчитав клиренс креатинина по Кокрофт-Голт или скорость клубочковой фильтрации по MDRD или CKD-EPI).
Пациентам, которым необходим прием пероральных антикоагулянтов, но Warfarin в подобранной дозе (МНО от 2 до 3) нельзя использовать вследствие трудностей поддержания терапевтического уровня гипокоагуляции (TTR<70%), невозможности тщательного контроля МНО, побочных эффектов, межлекарственного взаимодействия, рекомендуется принимать один из следующих неантогонистов витамина К: dabigatran, apixaban или rivaroxaban. Старт приема НОАК осуществляется после отмены Warfarin и достижения МНО<2.
У пациентов, принимающих dabigatran, apixaban или rivaroxaban отсутствует необходимость в рутинном контроле показателей свертывающей системы крови.
Dabigatran etexilate в дозе 150 мг 2 раза в день по сравнению с warfarin эффективнее снижает риск инсульта/системных эмболий, а также инсульта неуточненной этиологии, обладает сопоставимой безопасностью с точки зрения появления крупных кровотечений, использование его сопряжено с меньшими рисками возникновения геморрагического инсульта, внутричерепных кровоизлияний, общей частоты кровотечений и жизнеугрожающих кровотечений.
Dabigatran etexilate в дозе 110 мг 2 раза в день по сравнению с warfarin обладает не меньшей эффективностью по снижению риска инсульта/системных эмболий и достоверно большей безопасностью, вызывая меньшее количество крупных кровотечений, жизнеугрожающих кровотечений, геморрагических инсультов, внутричерепных кровоизлияний.
Apixaban по сравнению с warfarin обладает большей эффективностью в снижении риска инсультов/системных эмболий, более низким риском развития крупных кровотечений, геморрагических инсультов, внутричерепных кровоизлияний, а также снижает смертность от всех причин.
Apixaban пациентам с фибрилляцией предсердий назначают в дозе 5 мг два раза в день.
Необходимо снижать дозу Apixaban до 2,5 мг дважды в день у пациентов, обладающих двумя или более из следующих характеристик: возраст старше 80 лет; масса тела менее 60 кг или концентрация креатинина в плазме крови ≥133 мкмоль/л. Еще одним показанием для снижения дозы Apixaban до 2,5 мг дважды в день является клиренс креатинина от 15 до 30 мл/мин.
Rivaroxaban по сравнению с warfarin обладает не меньшей эффективностью по снижению риска инсульта/системных эмболий, сопоставимым риском крупных кровотечений, более низким риском геморрагических инсультов и внутричерепных кровоизлияний.
Rivaroxaban пациентам с фибрилляцией предсердий назначают в дозе 20 мг 1 раз в день.
Необходимо снижать дозу rivaroxaban до 15 мг 1 раз в день пациентам с клиренсом креатинина в диапазоне от 15 до 50 мл/мин.
Использование apixaban или rivaroxaban противопоказано у больных с клиренсом креатинина <15 мл/мин или тем пациентам, которым проводится гемодиализ.
Использование dabigatran противопоказано у больных с клиренсом креатинина <30 мл/мин или тем пациентам, которым проводится гемодиализ.
Эффективность и безопасность комбинации НОАК (dabigatran, apixaban или rivaroxaban) с антитромбоцитарными препаратами не исследована и не может рутинно применяться в практике вне рамок клинических исследований.
Выбор перорального антикоагулянта у пациента с фибрилляцией предсердий должен быть индивидуализированным и основываться на факторах риска, стоимости препарата, переносимости, потенциальным взаимодействии его с другими лекарственными препаратами, а также коморбидном состоянии.
В случае отказа от приема любых пероральных антикоагулянтов (warfarin, dabigatran, apixaban или rivaroxaban), назначение антитромбоицитарной монотерапии не является эффективным для профилактики рецидивов инсульта или ТИА.
Сроки начала терапии пероральными антикоагулянтами у больных, перенесших ишемический инсульт или ТИА (H. Diener):
- ТИА – в первые сутки, как только выполнено КТ головного мозга и исключен геморрагический тип инсульта;
- малый инсульт (NIHSS<8 баллов) – на 3-и сутки, если при исходном выполнении КТ головного мозга исключено кровоизлияние;
- средний инсульт (NIHSS-8–15 баллов) – на 6 сутки, с обязательным повторным выполнением КТ или МРТ головного мозга и исключением геморрагической трансформации ишемического инсульта;
- тяжелый инсульт (NIHSS>16 баллов) – на 12 сутки, с обязательным повторным выполнением КТ или МРТ головного мозга и исключением геморрагической трансформации ишемического инсульта.
Острый инфаркт миокарда и тромб в левом желудочке
Пациентам с ишемическим инсультом или ТИА, обусловленными ИМ или тромбом в левом желудочке, целесообразно назначение антагониста витамина К с уровнем МНО 2,0–3,0 на период от 3 месяцев до 1 года.
Дилятационная кардиомиопатия
Пациентам с ишемическим инсультом или ТИА и дилатационной кардиомиопатией может быть рекомендован как Warfarin (целевое значение МНО 2,5; интервал 2,0 – 3,0), так и антитромбоцитарная терапия для профилактики рецидивов.
Для пациентов с инсультом или ТИА, у которых при синусовом ритме существует кардиомиопатия с систолической дисфункцией (фракция выброса левого желудочка <35%), польза от Warfarin и НОАК не установлена.
Поражение нативных клапанов сердца
Пациентам с ишемическим инсультом или ТИА и ревматическим пороком митрального клапана, вне зависимости от наличия фибрилляции предсердий, обосновано назначение длительной терапии Warfarin (целевое значение МНО 2,5; интервал 2,0 – 3,0).
К Warfarin не следует рутинно добавлять антитромбоцитарные препараты, так как такая комбинация увеличивает риск кровотечений.
Пациентам с пролапсом митрального клапана и ишемическим инсультом или ТИА обосновано назначение антитромбоцитарной терапии.
Пациентам с митральной регургитацией и кальцинозом устья митрального клапана без фибрилляции предсердий может быть назначена антитромбоцитарная терапия или Warfarin (целевое значение МНО 2,5; интервал 2,0 – 3,0).
Пациентам с ишемическим инсультом или ТИА и поражением аортального клапана без фибрилляции предсердий обосновано назначение антитромбоцитарной терапии.
Пациентам с митральным стенозом умеренной или тяжелой степени ревматической этиологии показан прием Warfarin (целевые значения МНО 2–3 для неоперированного клапанного порока). Назначение НОАК противопоказано.
Искусственные клапаны сердца
Пациентам с фибрилляцией предсердий и механическим протезом клапанов сердца показан прием Warfarin (целевые значения МНО 2–3 — для искусственного клапана в аортальной позиции; 2,5–3,5 – для искусственного клапана в митральной позиции). Назначение НОАК противопоказано.
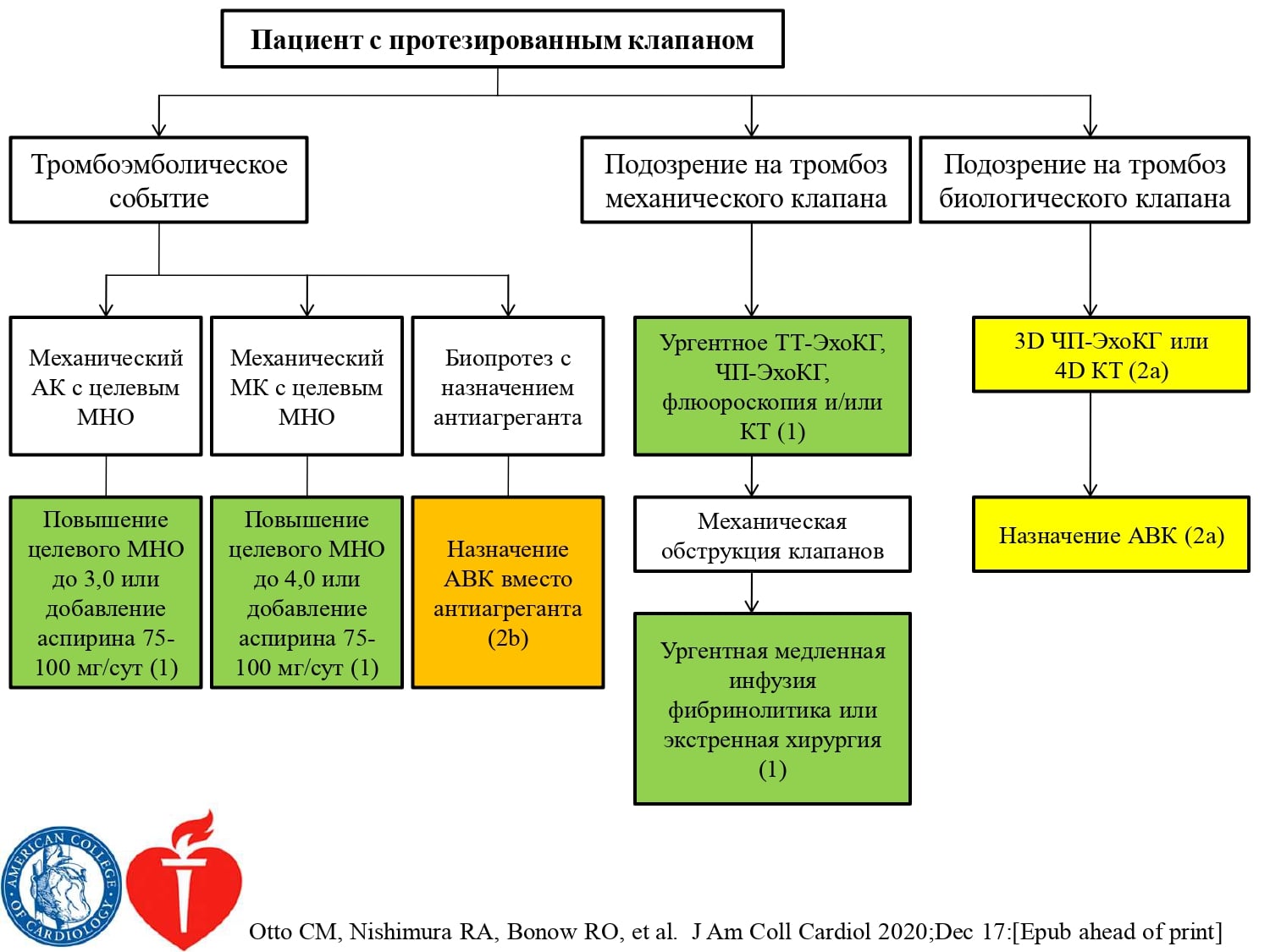
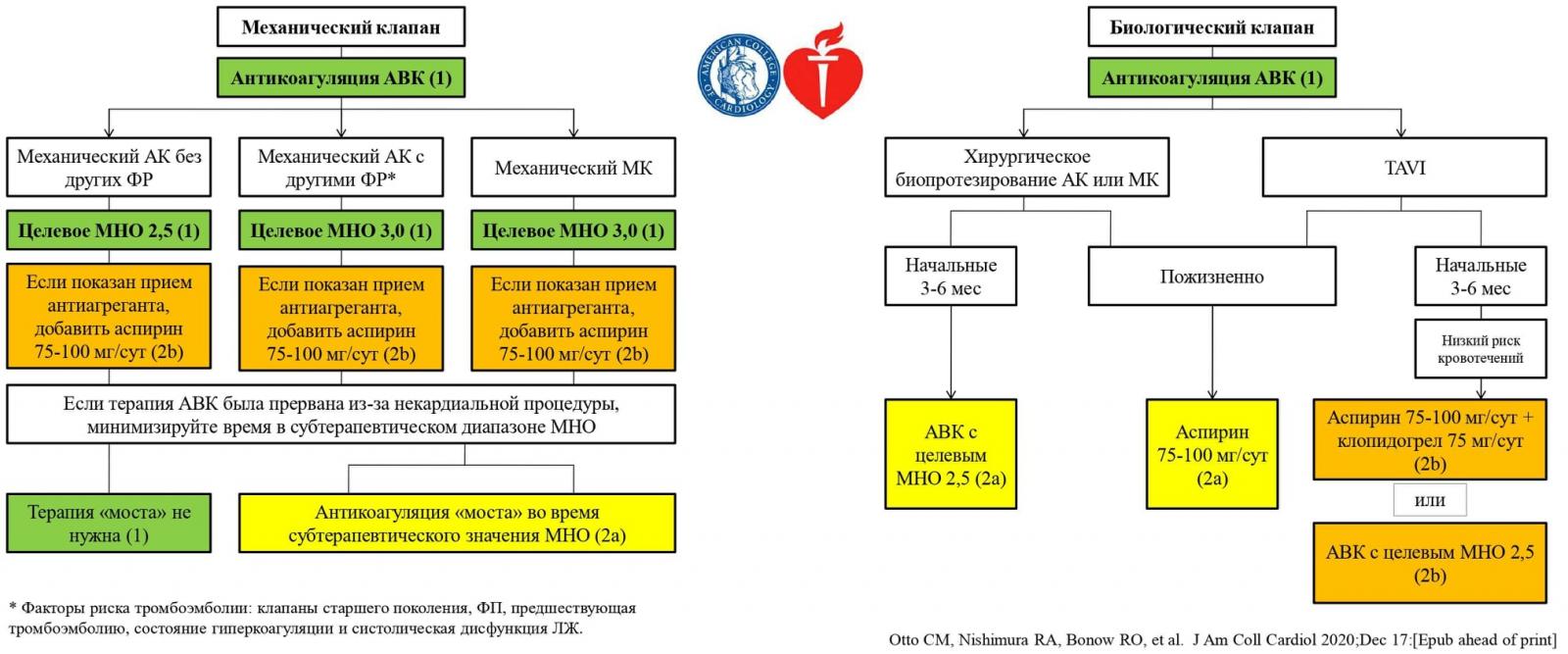
Пациентам с ишемическим инсультом или ТИА с биологическими протезами клапанов сердца, у которых не существует других источников кардиогенной эмболии, рекомендуется Warfarin (целевое значение МНО 2,5; интервал 2,0–3,0) на период от 3 до 6 месяцев.
Пациентам с искусственным клапаном сердца, ишемическим инсультом и системной эмболией, несмотря на адекватную терапию пероральными антикоагулянтами, целесообразно проведение поиска и коррекции другой возможной причины инсульта.
В настоящее время существует 2 тактики ведения таких пациентов: увеличение дозы Warfarin с поддержанием МНО на уровне 3,0 (в пределах 2,5–3,5) или назначение комбинации Aspirin в дозе 75–150 мг/сут и Warfarin с поддержанием МНО на уровне 2,5 (в пределах 2,0–3,0).
Некардиоэмболический инсульт
Пациентам, перенесшим некардиоэмболический ишемический инсульт (атеротромботический, лакунарный или инсульт неустановленной этиологии), показано назначение антитромбоцитарной терапии для профилактики повторного инсульта и повторных острых сосудистых событий.
Возможны следующие режимы антитромбоцитарной терапии:
- Clopidogrel (75 мг) в сутки;
- Aspirin 25 мг + Dipiridamol с медленным высвобождением 200 мг, 2 раза в сутки;
- Aspirin (50–325 мг) в сутки;
- Ticagrelor (90 мг) 2 раза в сутки.
Выбор режима антитромбоцитарной терапии должен быть индивидуальным и осуществляться на основании профиля факторов риска пациента, переносимости препаратов и других клинических характеристик. С целью снижения инцидентности головной боли при назначении комбинации Aspirin 25 мг + Dipiridamol с медленным высвобождением 200 мг необходимо: в первые 3 суток рекомендовать комбинацию Aspirin 25 мг + Dipiridamol с медленным высвобождением 200 мг однократно и дополнительно назначить Aspirin 50 мг; с 4-х суток комбинацию Aspirin 25 мг + Dipiridamol с медленным высвобождением 200 мг увеличить до регулярной дозы 2 раза в день, а Aspirin 50 мг отменить; при появлении головной боли или других симптомов непереносимости увеличение дозы откладывается до 14 суток.
Пациентам с противопоказаниями к терапии Aspirin рекомендуется назначение Clopidogrel.
Добавление Aspirin к Clopidogrel увеличивает риск кровотечений и не рекомендуется для широкого назначения пациентам. Исключения составляют больные ИИ и нестабильной стенокардией, или не-Q-образующим инфарктом миокарда, или недавним стентированием венечных артерий, которым необходимо назначать комбинацию Aspirin 75 мг/сут и Clopidogrel 75 мг/сут (длительность двойной антитромбоцитарной терапии зависит от типа имплантированного стента).
Для тех пациентов, у кого ишемический инсульт развился на фоне приема Aspirin — нет данных, что повышение дозы Aspirin приносит дополнительную пользу. Общепринято в данной ситуации повторно оценить патогенетические механизмы развития инсульта и назначить другие антитромботические препараты, хотя у таких пациентов не было изучено ни назначение одного из таких препаратов, ни их комбинации.
Для тех пациентов, у которых инсульт развился на фоне приема Aspirin, рекомендован прием Ticagrelor (90 мг 2 раза в сутки).
Коррекция факторов риска
Факторы риска (ФР) инсульта это различные клинические, биохимические, поведенческие и другие характеристики, свойственные отдельному человеку (и отдельным популяциям), а также внешние воздействия, наличие которых указывает на повышенную вероятность развития инсульта. Выявление и своевременная коррекция ФР является наиболее важным направлением борьбы с повторными инсультами.
ФР подразделяются на корригируемые и некоррегируемые.
К корригируемым ФР относятся:
- гипертоническая болезнь (ГБ);
- гиперлипидемия;
- сахарный диабет;
- курение;
- злоупотребление алкоголем;
- ожирение;
- синдром обструктивного апноэ сна;
- низкая физическая активность;
- метаболический синдром.
К некорригируемым ФР относятся:
- пол;
- возраст;
- этническая принадлежность;
- наследственность.
Гипертоническая болезнь
Под ГБ принято понимать хронически протекающее заболевание, основным проявлением которого является АГ, не связанная с наличием патологических процессов, при которых повышение АД обусловлено известными, в современных условиях часто устраняемыми причинами (симптоматические АГ).
Прием гипотензивных препаратов показан пациентам в остром периоде ишемического инсульта не ранее вторых суток. Максимальный подъем уровня систолического АД в первые сутки, не требующий гипотензивной коррекции — до 220 мм рт ст. Исключение составляют ситуации: необходимость проведения системного и/или интраартериального тромболизиса, наличие геморрагической трансформации.
Дополнительными показаниями к снижению уровня АД в острейшем пириоде ишемического инсульта являются: ОКС, сердечная недостаточность, диссекция аорты, внутричерепное кровоизлияние после тромболитической терапии, преэклампсия/эклампсия. У данных пациентов показано снижение АД не менее чем на 15%.
Абсолютные значения целевого АД и уровень снижения АД неизвестны и должны определяться индивидуально, но польза связывается со средним снижением АД на 10/5 мм рт. ст.
Пациенту должны быть рекомендованы следующие немедикаментозные методы снижения артериального давления: отказ от курения; нормализация массы тела; снижение потребления алкогольных напитков менее 24 г (в перерасчете на чистый спирт) алкоголя в сутки у мужчин и менее 12 г/сут – у женщин; увеличение аэробной физической нагрузки; снижение употребления поваренной соли до 5 г/сут; изменение режима питания с увеличением потребления овощей, фруктов, зерновых, обезжиренных молочных продуктов, уменьшения потребления животных жиров.
Больным, перенесшим инсульт или ТИА, рекомендовано назначение гипотензивной терапии в любой рациональной комбинации в зависимости от индивидуальных характеристик пациента с достижением целевого уровня АД ниже 140/90 мм рт ст.
Гиперлипидемия
Изменения концентраций липидных фракций само по себе, а также в сочетании с другими ФР приводит к развитию атеросклероза и повышению риска сердечно-сосудистых и цереброваскулярных заболеваний.
Пациентам с инсультом на фоне гиперлипидемии или атеросклероза церебральных артерий необходимо рекомендовать изменение образа жизни, диету с ограничением приема животных жиров и медикаментозную терапию статинами.
Для коррекции гиперлипидемии используются следующие группы лекарственных препаратов:
- ингибиторы 3-гидрокси-3-метилглутарил-коэнзим А-редуктазы (статины);
- фибраты;
- секвестранты желчных кислот;
- ниацин (никотиновая кислота);
- селективные ингибиторы поглощения холестерина (эзетимиб);
- ингибиторы пропротеиновой конвертазы субтилизин-кексинового типа 9 (ингибиторы PCSK9) – регуляторы экспрессии рецепторов ЛПНП.
Лечение проводится под динамическим мониторингом уровня ЛПНП.
Пациенты, перенесшие ИИ или ТИА, относятся к группе очень высокого риска. Целевой уровень ЛПНП у пациентов с очень высоким суммарным сердечно-сосудистым риском составляет <1,8 ммоль/л (<70 мг/дл); либо предполагает снижение уровня ЛПНП, по меньшей мере, на 50% по сравнению с исходным (если исходное значение составляет 1,8–3,5 ммоль/л (70–135 мг/дл)).
Пожилой возраст не должен являться препятствием для назначения статинов: показания к приему данного класса препаратов у пациентов пожилого возраста такие же, как и у лиц молодого возраста.
Лечение пациентов пожилого возраста целесообразно начинать с меньших доз препаратов, учитывая более высокий риск развития побочных реакций.
В случае если во время развития ИИ пациент принимал статины, необходимо продолжить данную гиполипидемическую терапию в острейшем периоде.
Предпочтительна терапия Atorvastatin в дозе 40 (80) мг/сут.
Статины являются относительно безопасной группой лекарственных препаратов. Риск развития нежелательных явлений, требующих отмены препаратов сопоставим с плацебо. Наиболее часто развивается патологическое повышение активности печёночных ферментов (0,3–5%, часто в начале лечения, носит дозозависимый характер; в ряде исследований сходные цифры при приёме плацебо).
В настоящее время оценка функции печени у пациентов, принимающих статины, требуется только до начала терапии, дальнейшие повторные исследования уровня печеночных ферментов через 8 недель.
Повышение АСТ или АЛТ в 3 раза является показанием к отмене препарата.
Пациентам после ишемического инсульта или ТИА с низким уровнем ЛПВП (менее 1 ммоль/л) можно рекомендовать прием Ac. Nicotinici или Gemfibrozilis.
У пациентов с ишемическим инсультом целесообразно рассмотреть возможность назначения препаратов группы PCSK9 в дополнение к оптимальной терапии статинами с целью снижения риска сердечно-сосудистой смерти, инфаркта миокарда или инсульта.
Сахарный диабет
У пациентов с ишемическим инсультом на фоне сахарного диабета рекомендован более жесткий контроль АД и уровня липидов. Препаратами выбора для антигипертензивной терапии у данных больных являются ингибиторы АПФ и блокаторы кальциевых каналов.
Необходимо диетой и медикаментозной терапией добиться нормогликемии у данной категории больных с целью уменьшения микро — и макроангиопатии.
Целевое значение гликозилированного гемоглобина (HbA1c) у больных инсультом составляет <7%.
Выбор в пользу приема пероральных сахароснижающих средств и/или заместительном введении инсулина в специально подобранном, близком к физиологической секреции режиме, в каждом отдельном случае осуществляется с учетом индивидуальных особенностей пациента.
Ожирение и низкая физическая активность
Ожирение диагностируют у пациентов с индексом массы тела >30 кг/м2.
Лицам, страдающим ожирением, рекомендуется придерживаться диеты для снижения веса.
Пациентам после ишемического инсульта или ТИА, способным к физической активности, можно рекомендовать минимум 30 минут физических упражнений умеренной интенсивности 7 раза в неделю (например, энергичная ходьба, тренажер, велосипед).
Пациентам с инвалидизацией после ишемического инсульта в начале подбора режима нейрореабилитационных упражнений необходимо проводить занятия под руководством реабилитологов.
Синдром обструктивного апноэ сна
Синдром обструктивного апноэ сна — это состояние, характеризующееся наличием храпа, периодическим спадением верхних дыхательных путей на уровне глотки и прекращением легочной вентиляции при сохраняющихся дыхательных усилиях, снижением уровня кислорода в крови, грубой фрагментацией сна и избыточной дневной сонливостью.
Факторами, способствующими развитию СОАС, являются ожирение, мужской пол, возраст, семейный анамнез, гипотиреоз, назальная обструкция, курение.
Во время сна у людей, страдающих СОАС, происходят характерные преходящие окклюзии верхних дыхательных путей, которые приводят к эпизодам частичного (гипопноэ) или полного (апноэ) прекращения (прерывания) потока воздуха. При тяжелых формах СОАС может отмечаться до 400–500 остановок дыхания за ночь общей продолжительностью до 3–4 часов, что ведет к острому и хроническому недостатку кислорода во время сна. Что, в свою очередь, существенно увеличивает риск развития артериальной гипертензии, сахарного диабета, нарушений ритма сердца, инфаркта миокарда, инсульта и внезапной смерти во сне. Каждая остановка дыхания сопровождается частичным или полным пробуждением мозга, что приводит к резкому ухудшению качества сна.
Клинически СОАС проявляется громким храпом, замечаемым посторонними, остановками дыхания во время сна; пациенты предъявляют жалобы на ночные пробуждения с ощущением нехватки воздуха, отсутствие ощущения полноценного ночного отдыха, дневную сонливость.
С целью диагностики СОАС проводят кардио-респираторный мониторинг (КРМ) или полисомнографию (ПСГ).
Общепризнанным критерием степени тяжести СОАС является частота апноэ и гипопноэ в час – индекс апноэ/гипопноэ (ИАГ).
Классификация тяжести СОАС представлена в таблице 1.
Таблица 1. Классификация тяжести СОАС у взрослых.
| Тяжесть СОАС | ИАГ |
|---|---|
| Легкая степень | от ≥5 до <15 |
| Умеренная (средняя) степень | от ≥15 до <30 |
| Тяжелая степень | ≥30 |
Выделяют следующие основные направления терапии СОАС:
- общепрофилактические мероприятия;
- обеспечение свободного носового дыхания;
- применение электромеханических подбуживающих (стимулирующих пробуждение) устройств;
- применение внутриротовых приспособлений;
- применение фармакологических средств, облегчающих храп;
- оперативное лечение (хирургическое, лазерное);
- лечение методом неинвазивной вспомогательной вентиляции постоянным положительным давлением в дыхательных путях.
Методом выбора при лечении СОАС любой этиологии в настоящее время является Continuous Positive Airway Pressure-терапия (СРАР)— неинвазивная вспомогательная вентиляция постоянным положительным давлением в дыхательных путях во время сна через маску. Данная методика является основной при терапии СОАС умеренной и тяжелой степени.
Суть данного метода состоит в поддержании на продолжении всего дыхательного цикла положительного давления в дыхательных путях, вследствие чего создается препятствие для их спадения и соответственно устраняется субстрат СОАС.
Курение
Пациентам, перенесшим инсульт, необходимо рекомендовать отказаться от курения.
Желательно избегать пассивного курения.
Психологическая поддержка, никотин-содержащие продукты и препараты для отмены курения эффективно помогают отказаться от курения.
Рекомендовано консультирование, использование заменителей никотина совместно с прекращением курения
Необходима поведенческая терапия в период стационарного лечения, направленная на отказ пациента от курения
Рекомендовано в период госпитализации применение медикаментозной коррекции никотиновой зависимости с использованием varenicline
Пациентам после ишемического инсульта, необходимо избегать «пассивного» курения.
Злоупотребление алкоголем
Пациентам, перенесшим инсульт, необходимо рекомендовать отказаться от злоупотребления алкоголем.
Ежедневный прием низких доз алкоголя (24 мг в перерасчете на 100% этиловый спирт для мужчин и 12 мг для женщин) ассоциируется с редукцией риска развития инсульта.
Пациентам, не употреблявшим алкоголь до инсульта, не следует начинать его прием.
Метаболический синдром
Метаболический синдром характеризуется сочетанием трёх и более нарушений: высокого уровня гликемии натощак, артериальной гипертензии, низкого уровня липопротеидов высокой плотности, высокого уровня триглицеридов и абдоминального ожирения.
У пациентов с метаболическим синдромом терапия должна включать изменение образа жизни (диета, физические нагрузки, снижение веса) для снижения риска повторных инсультов.
Стено-окклюзирующие поражения церебральных артерий
Внечерепные стенозы сонных артерий
При выявлении симптомных стенозов сонных артерий более 70% по данным ультразвукового допплеровского сканирования брахиоцефальных артерий и более 50% по данным КТ-ангиографии или церебральной ангиографии, показано хирургическое лечение (КЭ или ТБАС).
Пациентам с симптомным стенозом менее 50%, КЭ или транслюминальная балонная ангиопластика со стентированием (ТБАС) внутренних сонных артерий (ВСА) не показаны.
Так как при атеротромботическом патогенетическом подтипе ИИ риск повторного инсульта крайне высок, КЭ необходимо выполнять в ранние сроки.
Пациентам с легким неинвалидизирующим инсультом (по модифицированной шкале Ранкина 0–2) целесообразно выполнять операцию на сонных артериях в интервале между 48 часами и 7 сутками после острого события, если нет противопоказаний к ранней реваскуляризации.
Остальным пациентам целесообразно выполнять операцию на сонных артериях в течение первых двух недель от дебюта инсульта.
Антитромбоцитарные препараты необходимо принимать до и после операции.
ТБАС является альтернативой КЭ для симптомных пациентов со средним или низким риском осложнений эндоваскулярного вмешательства.
Стентирование сонных артерий предпочтительнее КЭ в следующих случаях: существует повышенный риск интраоперационных осложнений при КЭ, имеются противопоказания к КЭ, стеноз располагается в хирургически недоступном месте, рестеноз после КЭ, стеноз после лучевой терапии. Пациенты, перенесшие стентирование, должны получать комбинацию Clopidogrel 75 мг и Aspirin 75 мг непосредственно до, во время и как минимум в течение 1 месяца после вмешательства.
И КЭ, и ТБАС могут выполняться у пациентов разных возрастных групп, но у молодых пациентов предпочтительнее ТБАС, у пожилых пациентов – КЭ.
Операции на сонных артериях должны выполняться только в центрах, в которых показатель периоперационных осложнений (любой инсульт, инфаркт миокарда или смерть) не превышает 6%.
Пациентам с инсультом, которым выполнена КЭ (ТБАС) показана терапия антитромбоцитарными препаратами и статинами, а также коррекция факторов риска.
Внечерепные стенозы артерий вертебрально-базилярного бассейна
Всем пациентам с инсультом или ТИА и стенозом позвоночной артерии, рекомендуется оптимальная лекарственная терапия, которая должна включать антитромбоцитарные препараты, статины, модификацию факторов риска.
Эндоваскулярное и открытое хирургическое лечение можно рекомендовать пациентам с наличием симптомного внечерепного стеноза позвоночной артерии, у которых инсульт или ТИА развились, несмотря на оптимальную медикаментозную терапию (включая антитромбоцитарные препараты, статины и удовлетворительный контроль факторов риска).
Внутричерепные стенозы
У пациентов с инсультом или ТИА вследствие 50–99% стеноза крупной внутричерепной артерии, отдается предпочтение Aspirin, а не варфарину. Оптимальная доза Aspirin в этой популяции не установлена, но на основании общих данных по безопасности и эффективности рекомендуется ежедневная доза Aspirin от 75 мг до 150 мг.
У пациентов с инсультом или ТИА вследствие 50–99% стеноза крупной внутричерепной артерии имеет смысл длительное поддержание АД <140/90 мм рт. ст. и уровня ЛПНП <1,8 ммоль/л.
Для пациентов с недавним инсультом или ТИА (в течение 30 дней), связанным с тяжелым интракраниальным стенозом (70% — 99%) магистральной мозговой артерии, может быть оправдано добавлениеклопидогреля 75 мг /сут к аспирину в течение 90 дней.
Чрезкожная транслюминальная ангиопластика и/или стентирование может быть использована у пациентов с симптомными интракраниальными стенозами ≥50%. В настоящее время недостаточно доказательной базы для того, чтобы рутинно применять данное вмешательство, поэтому решение о тактике лечения у пациентов с интракраниальными стенозами должно применяться индивидуально.
Пациентам с инсультом или ТИА вследствие 50–99% стеноза крупной внутричерепной артерии операция экстра-интракраниального шунтирования (создание анастомоза между ветвями поверхностной височной и средней мозговой артерии) не рекомендуется.
Окклюзии церебральных артерий
Пациентам с окклюзиями церебральных артерий показана консервативная терапия, направленная на коррекцию сосудистых факторов риска. Операция экстра-интракраниального шунтирования обладает высоким риском интраоперационных осложнений и не имеет преимуществ перед консервативным лечением.